微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
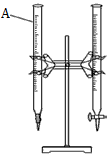
1、填空题 (1)下图是用已知浓度的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前、后的盛放盐酸的滴定管中液面的位置。请回答:
①仪器A的名称是 ________________________ ;
②盐酸的体积读数:滴定前读数为____________mL,所用盐酸的实际体积为____________mL 。
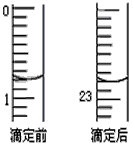
(2)我国是最早使用铜及其合金的国家之一,黄铜就是一种铜锌合金。已知下列反应:Zn+CuSO4=
ZnSO4+Cu,若利用该反应设计成原电池,则其中负极材料是________,正极反应式是____________;若反应结束后有32g铜析出,则导线中有________mol电子从________(填电极名称)流向________(填电极名称)。某学生想利用电解原理在锌表面镀上一层铜,则阳极材料是__________,阴极材料是__________,所用电镀液是_____________,阳极电极反应式是______________
参考答案:(1)①碱式滴定管;②0.80;22.00
(2)锌
本题解析:
本题难度:一般
2、选择题 如图把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池。某实验兴趣小组做完实验后,在读书卡上的记录如下所示,则卡片上的描述合理的是(??)
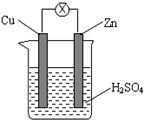
卡片号:2013.4
实验后的记录:
①Cu为阳极,Zn为阴极?②Cu极上有气泡产生
③SO42-向Cu极移动?④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子流向是:Cu  Zn
Zn
⑥正极反应式:Cu + 2e- = Cu2+
A.①②③
B.②④
C.④⑤⑥
D.③④⑤
参考答案:B
本题解析:
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,铜是正极,溶液中的氢离子在正极得到电子,①③⑤错误,②④正确,答案选B。
点评:该题主要是考查学生对原电池原理的熟悉了解程度,意在检验学生灵活运用基础知识解决实际问题的能力。该题的关键是明确原电池的工作原理,并能结合题意灵活运用即可。
本题难度:简单
3、填空题 (8分)如图所示的原电池中,回答下列问题
(1)负极材料??????????????
(2)写出电极反应式:正极:??????????????????;负极:????????????????????。
(3)写出电极反应总反应式??????????????????????????????????????
(4)电子由??????极流向?????极(填写Zn或Cu)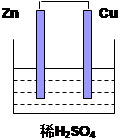
参考答案:(1)Zn? (2分)??????(2)2H++2e-=H2
本题解析:考查原电池的有关判断和应用。在原电池中较活泼的金属作负极,失去电子,发生氧化反应,所失去的电子经导线传递到正极上。锌比铜活泼,所以锌是负极,失去电子。铜是正极,溶液中的氢离子在正极得到电子,发生还原反应生成氢气。
本题难度:一般
4、填空题 (6分)(1)X、Y、Z三种金属,X、Y组成原电池,X是负极;把Y放在Z的硝酸盐溶液中,Y表面有Z析出。其活泼顺序是_________________;
(2)由氢气和氧气反应生成1mol水蒸气放热241.8 kJ,写出该反应的热化学方程式:___________________________??????????????????????_______。
(3)下列各情况,在其中Fe片腐蚀由快到慢的顺序是???????????????????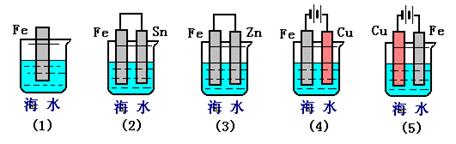
参考答案:(1)X>Y>Z
(2)2H2(g)+O2
本题解析:(1)在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。X、Y组成原电池,X是负极,因此X的金属性强于Y;Y放在Z的硝酸盐溶液中,Y表面有Z析出,则Y的金属性强于Z,所以金属性强弱顺序是X>Y>Z。
(2)氢气和氧气反应生成1mol水蒸气放热241.8 kJ,所以该反应的热化学方程式是)2H2(g)+O2(g)=2H2O(g)?△H=-483.6 kJ・mol-1。
(3)根据装
本题难度:一般
5、选择题 电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-===ZnO+H2O; Ag2O+H2O+2e-===2Ag+2OH-,下列说法正确的是
A.Zn为正极,Ag2O为负极
B.Ag2O发生还原反应
C.原电池工作时,正极区溶液pH值减小
D.原电池工作时,负极区溶液pH值增大
参考答案:B
本题解析:
试题分析:;A、据电极反应式Zn被氧化,发生氧化反应,为原电池的负极,则正极为Ag2O,错误;B、因为Ag2O为正极,所以得电子发生还原反应,正确;C、原电池工作时,正极反应Ag2O+H2O+2e-=2Ag+2OH-,正极区溶液PH值增大,错误;D、原电池工作时,负极反应Zn+2OH--2e-=ZnO+H2O,溶液PH值减小,错误。
考点:考查原电池工作原理。
本题难度:一般