微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是[???? ]
A.其它条件相同时,增大反应物浓度使分子获得能量,活化分子百分数提高,反应速率增大
B.判断过程的自发性能确定过程能否发生和过程发生的速率
C.体系有自发地向混乱度增加(即熵增)的方向转变的倾向,这是自然界的普遍规律
D.催化剂不影响反应活化能,从而只影响反应速率,不影响化学平衡
参考答案:C
本题解析:
本题难度:一般
2、选择题 一定量的盐酸跟过量铁粉反应时,为了减慢反应速率,且不影响生成H2的总量,可以向盐酸中加入适量的
A.固体NaOH
B.Na2SO4溶液
参考答案:
本题解析:
本题难度:一般
3、选择题 反应C(s)+H2O(g)  CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )。
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )。
①增加C的量 ②将容器的体积减小一半 ③保持体积不变,充入氮气使体系的压强增大 ④保持压强不变,充入氮气使体系的体积增大
A.①②
B.②③
C.①③
D.③④
参考答案:C
本题解析:C为固态物质,增加其用量对反应速率几乎无影响;容器的体积减小,则体系的压强增大,反应速率增大;充入氮气使体系的压强增大,但由于容器体积不变,反应混合物中各成分的浓度不变,所以化学反应速率不变;保持压强不变,充入氮气使体系的体积增大,反应混合物中各成分的浓度减小,反应速率变慢。
本题难度:一般
4、填空题 如下图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题。
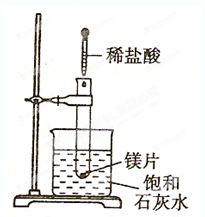
⑴实验中观察到的现象是________???????____________?_______________
_____________________????______????????????????????????_________。
⑵产生上述现象的原因是____?????????????????_______?______________
_____________________?????_____????????????????????????_________。
⑶写出有关反应的离子方程式_???????????????_______________________。
⑷由实验推知,MgCl2溶液和H2的总能量____________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
参考答案:(1)①镁片上有大量气泡产生;②镁片逐渐溶解;③烧杯中溶液变
本题解析:镁是活泼的金属,能和盐酸反应生成氢气和氯化镁。该反应是放热反应,说明反应物的总能量高于生成物的总能量。溶液温度升高,但由于Ca(OH)2在水中溶解度水温度升高而减小,所以析出Ca(OH)2固体。
本题难度:一般
5、选择题 下列有关说法正确的是
A.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解
B.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
C.N2(g)+3H2(g) 2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大
2NH3(g) ΔH<0,其他条件不变升高温度,平衡时氢气转化率增大
D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的ΔS<0
参考答案:A
本题解析:
试题分析:A.CaSO4微溶于水,在溶液中存在沉淀溶解平衡,当加入饱和Na2CO3溶液浸泡时会发生沉淀反应形成CaCO3沉淀,促进CaSO4的溶解,沉淀转化为CaCO3,再加入盐酸CaCO3发生反应产生氯化钙、水和CO2,达到溶解沉淀的目的,正确;B.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量CuSO4溶液或CuCl2溶液,但是由于在酸性环境中NO3-表现强氧化性,不能产生氢气,错误;C.N2(g)+3H2(g) 2NH3(g)的正反应是放热反应,在其他条件不变时,升高温度,根据平衡移动原理,平衡逆向移动,氢气转化率减小,错误;D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,ΔS<0,则该反应的ΔH<0,错误。
2NH3(g)的正反应是放热反应,在其他条件不变时,升高温度,根据平衡移动原理,平衡逆向移动,氢气转化率减小,错误;D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,ΔS<0,则该反应的ΔH<0,错误。
考点:考查沉淀的溶解与转化、影响化学反应速率、化学平衡的因素及反应自发进行的判据的知识。
本题难度:一般