微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 23.(10分)下表是某超市出售的加碘食盐的有关说明:
| 精制盐、碘酸钾
|
含???碘???量
| 45±5mg/kg
|
储?藏?方?法
| 通风、防潮
|
食?用?方?法
| 根据烹调所需适量加入
???某研究性学习小组欲通过实验检验该碘盐中是否含碘:
(1)首先取该食盐样品配制室温下的饱和溶液:向200 mL蒸馏水中加入75.0g该食盐样品,加热并搅拌,直到完全溶解。冷却至室温。(已知室温条件下氯化钠溶解度为36 g)
在加热过程中需要用到的仪器有铁架台、酒精灯、铁圈、____________、烧杯和玻璃棒。冷却至室温过程中若出现____________________(填现象),则证明其为饱和溶液。
(2)甲同学先向该饱和食盐溶液中加入1mol/L的KI溶液和几滴淀粉溶液,然后加入0.1mol/L稀硫酸,振荡,溶液变为蓝色。该实验发生的化学反应中氧化剂与还原剂的物质的量之比为_______________。请在下图中画出参加反应的IO3―的物质的量和析出的I2单质的物质的量的关系曲线。
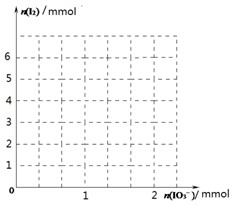
(3)乙同学认为甲同学的实验方案不严谨,他提出如下假设:空气中的氧气可能参与反应,使溶液变蓝。反应的离子方程式为:_____________________________________。请你设计实验方案验证乙同学的假设是否正确:?????????????????????????????????????????????????????。
参考答案:(10分)
(1)石棉网??固体析出(每空1分,共2分
本题解析:(1)对于底面积较大的容器加热时要垫石棉网;
饱和溶液:在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时所得的溶液;
(2)由IO3-+5I-+6H+=3I2+3H2O可知反应中氧化剂与还原剂的物质的量之比为1:5;
而IO3-与生成的I2的物质的量比为1:3
(3)I―还原性很强,在常温下即可被氧气氧化为碘。
本题难度:一般
2、选择题 除去下列各组物质中的杂质(括号内为杂质),采用的方法不正确的是( )
A.NaCl(NH4Cl)加热
B.FeCl2溶液(FeCl3)加铁粉
C.AlCl3溶液(MgCl2)加氨水
D.Na2CO3(NaHCO3)加热
参考答案:A.氯化铵不稳定,在加热条件下易分解生成氨气和氯化氢,氯化钠
本题解析:
本题难度:一般
3、选择题 矿盐的主要成分是NaCl,还混有SO42-等其他可溶性杂质的离子。下列有关说法正确的是
A.用矿盐生产食盐,除去SO42-最合适的试剂是Ba(NO3)2
B.工业上通过电解氯化钠溶液制备金属钠和氯气
C.室温下,AgCl在水中的溶解度小于在食盐中的溶解度
D.用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液
参考答案:D
本题解析:
试题分析:A项会引入NO3-,错误;B项制备钠和氯气,电解熔融氯化钠,错误;AgCl在水中的溶解度大于在食盐中的溶解度,错误。
本题难度:一般
4、选择题 “碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).
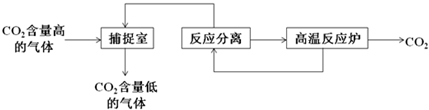
下列有关该方法的叙述中正确的是( )
A.能耗大是该方法的一大缺点
B.整个过程中,只有一种物质可以循环利用
C.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤
D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品
参考答案:A.碳酸钙的分解在高温条件下进行,消耗能量,故A正确;
本题解析:
本题难度:一般
5、选择题 下列除去杂质的方法正确的是
A.除去CO2中混有的CO:将混合气体通过装有NaOH溶液的洗气瓶
B.除去铜器表面的铜绿:用稀硝酸浸泡,再用水冲洗
C.除去KNO3溶液中少量NaCl:加水溶解,蒸发结晶,趁热过滤
D.除去Mg(OH)2固体中少量Ca(OH)2:加入足量MgCl2溶液,充分搅拌后过滤
参考答案:D
本题解析:略
本题难度:一般
|