微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关化学用语表示正确的是
A.羧基的结构简式:HCOO-
B.质子数为6、质量数为14的原子: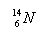
C.CCl4分子的电子式: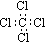
D.硫离子的结构示意图: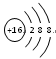
参考答案:D
本题解析:A 错误,羧基的结构简式:-COO-
B 错误,质子数为6、质量数为14的原子:614C
C 错误,氯原子也要画出最外层电子数
D 正确。
本题难度:简单
2、选择题 取19.2g铜跟少量的浓硝酸反应,铜全部溶解后,收集到NO2、NO混合气体的体积11.2L(标准状况),反应消耗硝酸的物质的量是
A.0.5mol
B.0.8mol
C.1.1mol
D.1.2mol
参考答案:C
本题解析:
试题分析:19.2克铜为0.3摩尔,反应后生成0.3摩尔硝酸铜,含有0.6摩尔的硝酸根离子,气体为0.5摩尔,根据氮原子守恒,总共氮原子为0.6+0.5=1.1摩尔,所以硝酸为1.1摩尔,选C。
考点:铜与硝酸反应,原子守恒。
本题难度:一般
3、选择题 下列化学用语书写正确的是 ?
A.氯原子的结构示意图: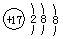
B.作为相对原子质量测定标准的碳核素:614 C
C.氯化镁的电子式: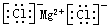
D.用电子式表示氯化氢分子的形成过程: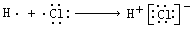
参考答案:C
本题解析:
试题分析:A、因氯原子结构中最外层电子数为7,故A错误;
B、相对原子质量的测定是以612C为标准进行计算的,故B错误;
C、氯化镁为离子化合物,在形成化合物时镁原子失去电子变为镁离子,氯原子等到电子变为氯离子,故C正确;
D、因HCl为共价化合物,则在HCl中的电子式中不会有氢离子和氯离子,故D错误;
故选C。
点评:本题考查化学用语,学生应注意原子的最外层电子数来分析形成的化合物,离子化合物中有离子,共价化合物中一定没有离子。
本题难度:一般
4、选择题 以下化学用语正确的是
A.乙烯的结构式:CH2=CH2
B.乙酸乙酯的分子式:C4H8O2
C.CO2的电子式:O::C::O
D.明矾的化学式:Fe2(SO4)3?7H2O
参考答案:B
本题解析:A.乙烯的结构简式:CH2=CH2?????B.乙酸乙酯的分子式:C4H8O2
C.CO2的电子式 :??????D.明矾的化学式:KAl(SO4)2?12H2O
:??????D.明矾的化学式:KAl(SO4)2?12H2O
本题难度:简单
5、填空题 (14分)镍是一种十分重要的有色金属,但粗镍中一般含有Fe、Cu及难与酸、碱溶液反应的不溶性杂质而影响使用。现对粗镍进行提纯,具体的反应流程如下:
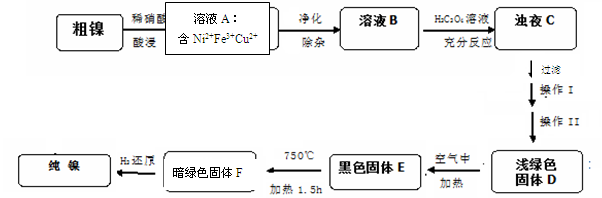
已知:
①2Ni2O3(黑色) 4NiO(暗绿色) + O2↑
4NiO(暗绿色) + O2↑
②
物质
| CuS
| Cu(OH)2
| Ni(OH)2
| NiS
|
Ksp
| 8.8×10-36
| 2.2×10-20
| 5.48×10-16
| 3.2×10-19
根据信息回答:
(1)28Ni在周期表中的第 周期;镍与稀硝酸反应的离子方程式为 。实验表明镍的浸出率与温度有关,随着温度升高镍的浸出率增大,但当温度高于70℃ 时,镍的浸出率又降低,浸出渣中Ni(OH)2含量增大,其原因为 ;
(2)在溶液A的净化除杂中,首先将溶液A煮沸,调节PH=5.5,加热煮沸5min,静置一段时间后,过滤出Fe(OH)3。为了得到纯净的溶液B还需要加入以下物质 进行除杂(填正确答案标号)。
A、NaOH B、Na2S C、H2S D、NH3
参考答案:
本题解析:
本题难度:一般
|