��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ܱ������н���N2��3H2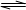 2NH3��Ӧ����ʼʱN2��H2�ֱ�Ϊ10mol��30mol�����ﵽƽ��ʱN2��ת����Ϊ30%������NH3��Ϊ��ʼ��Ӧ���Ӧ������������Ӧ��ͬʱ��Ҫʹ�䷴Ӧ�ﵽƽ��ʱ����ɳɷֵ����ʵ���������ǰ����ͬ����NH3����ʼ���ʵ���������ת������ȷ���ǣ�������
2NH3��Ӧ����ʼʱN2��H2�ֱ�Ϊ10mol��30mol�����ﵽƽ��ʱN2��ת����Ϊ30%������NH3��Ϊ��ʼ��Ӧ���Ӧ������������Ӧ��ͬʱ��Ҫʹ�䷴Ӧ�ﵽƽ��ʱ����ɳɷֵ����ʵ���������ǰ����ͬ����NH3����ʼ���ʵ���������ת������ȷ���ǣ�������
A��40mol��35%
B��20mol��30%
C��20mol��70%
D��10mol��50%
2������� ��һ���¶��£�4L�ܱ������ڴ��ڷ�Ӧ2N�TM����������M������N�����ʵ�����ʱ��仯��������ͼ��ʾ��
��1���Ƚ�t2ʱ�̣����淴Ӧ���ʴ�СV��______V�森
��2����t2=2min�����㷴Ӧ��ʼ��t2ʱ�̣�M��ƽ����ѧ��Ӧ����Ϊ��______��
��3��t1��t2��ȣ���Ӧ����______��������ԭ����______����֪�÷�Ӧ�Ƿ��ȷ�Ӧ����N������______M������ ������ڡ�����С�ڡ��������ڡ���
3��ѡ���� ������Ӱ�컯ѧ��Ӧ���ʵ����������͵���[???? ]
A��þ��п�ֱ�����ͬŨ�ȵ����ᷴӦ��þ����H2�����ʿ�
B��H2S�ڿ�����ȼ�ճʵ���ɫ���棬�ڴ�������ȼ�ճ�����ɫ����
C���ü��ȵķ�����ˮ�е��������������
D����ۼӹ����ڳ����۳���������ᷢ����ը
4��ʵ���� ��ͬѧ��ͨ��ʵ��̽��ͬ����Ԫ�����ʵĵݱ���ɣ��Լ�Ӱ�컯ѧ��Ӧ���ʵ����ء�����Ƶ�ʵ�鷽�����£����������д���������������ۡ�ʵ�����ṩ���Լ���п�顢п�ۡ����������ۡ�ͭ����NaBr��Һ��NaI��Һ�����Ƶ���ˮ��1mol/?���ᡢ3mol/L������
��1��̽��ͬ����Ԫ�����ʵĵݱ����
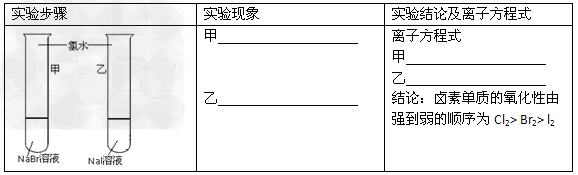
�����ۡ���ͬѧ��Ƶ�ʵ�鷽���ĺ�������___________������ţ�
A.?�dz����� B.?���ֺ��� C.?��ȫ������
����������ơ���һ������A������������������B��C�������ʵ�黹��Ҫ���Լ���___________��
��2��̽��Ӱ�컯ѧ��Ӧ���ʵ�����

��ͬѧ����ʵ�����ݺͽ������������⣬������__________��
��3����������ԭ���ԭ�������ʵ�飬�Ƚ�ͭ�����Ľ�����ԡ�����ʵ��װ��ͼ�������������������������д���缫��Ӧʽ��
��
�ڵ缫��Ӧʽ ____________________________��____________________________
5��ѡ���� �ں����ܱ��������еĿ��淴Ӧ��MgSO4(s) + CO(g)  ?MgO(s) + CO2(g) + SO2(g)��Q�����з�����������
?MgO(s) + CO2(g) + SO2(g)��Q���������������
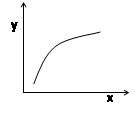
A����ƽ�ⳣ��Kֵ���ƽ���ƶ�ʱv���ȼ�С������
B�������й������ʵ��������ٸı䣬��Ӧ����ƽ��״̬
C����x��ʾ�¶ȣ�y�ɱ�ʾƽ��ʱ���������ܶ�
D����x��ʾCO���ʵ�����y�ɱ�ʾƽ��ʱCO2��CO���ʵ���֮��