��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����йػ�ѧ��Ӧ���ʵ�˵���У���ȷ����
A����Ƭ��ϡ������ȡ����ʱ������NaNO3�����Na2SO4���嶼��Ӱ����������������
B����������пƬ�ֱ���ͬ�����ͬ���ʵ���Ũ�ȵ����ᡢ���ᷴӦ����Ӧ���ʲ����
C��SO2�Ĵ�������һ�����ȷ�Ӧ�����������¶ȣ���Ӧ���ʼ���
D�����뷴Ӧ���λ����ڻ���Ӱٷ�������ѧ��Ӧ��������
�ο��𰸣�B
���������A����Ƭ��ϡ������ȡ����ʱ������NaNO3���岻�ٲ���������A�������ʵ���Ũ����ͬ�����ᡢ�����У�������������Ũ�ȴ�Ӧ�Ŀ죬B�ԡ���Ӧ�����Ƿ��Ȼ������ȣ�ֻҪ�����¶ȣ���Ӧ���ʶ���ӿ죬C�������뷴Ӧ���λ����ڻ���Ӱٷ������䣬D����
�����Ѷȣ�һ��
2��ѡ���� ��0.6 mol X�����0.4 mol Y��������1L������ʹ���Ƿ������·�Ӧ��3X(g)��Y(g) ?nZ(g)��2W(g), 5 minĩ������0.3 mol W������֪��ZŨ�ȱ仯����ʾ�ķ�Ӧƽ������Ϊ0.03 mol��L��1��min��1����������Ӧ��Z����ķ�Ӧ����ʽϵ��n��ֵ��(��)
?nZ(g)��2W(g), 5 minĩ������0.3 mol W������֪��ZŨ�ȱ仯����ʾ�ķ�Ӧƽ������Ϊ0.03 mol��L��1��min��1����������Ӧ��Z����ķ�Ӧ����ʽϵ��n��ֵ��(��)
A��1
B��2
C��3
D��4
�ο��𰸣�A
�����������Ӧ3X(g)��Y(g) ?nZ(g)��2W(g),
?nZ(g)��2W(g),
��ʼ���ʵ���? 0.6??? 0.4??????? 0????? 0
�仯���ʵ���? 0.45? 0.15?????? 0.15n??? 0.3
5min�����ʵ���0.15? 0.25????? 0.15n??? 0.3
�����Ѷȣ�һ��
3��ѡ���� ��2A��B?2C��D��Ӧ�У���ʾ�÷�Ӧ���������ǣ�������
A��v��A��=0.8mol?L-1?s-1
B��v��B��=0.3mol?L-1?s-1
C��v��C��=0.6mol?L-1?s-1
D��v��D��=0.5mol?L-1?s-
�ο��𰸣���ת��ΪA���ʱ�ʾ�����ʽ��бȽϣ�����2A+B?2C+D��<
���������
�����Ѷȣ���
4��ѡ���� ������̼��ƹ��巴Ӧʱ�����д�ʩ��ʹ����ķ�Ӧ�������Լӿ���ǣ�������
A������̼��Ƶ���
B���������������һ��
C��������������룬Ũ�ȼӱ�
D���¶�����
�ο��𰸣�A������̼��Ƶ����������ı�Ũ�ȣ���Ӧ���ʲ��䣬��A����<
���������
�����Ѷȣ�һ��
5������� �¶�ΪTʱ����2.0 L�����ܱ������г���1.0 mol PCl5����ӦPCl5(g)��PCl3(g)��Cl2(g)����һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
t/s
| 0
| 50
| 150
| 250
| 350
|
n(PCl3)/mol
| 0
| 0.16
| 0.19
| 0.20
| 0.20
?
����˵����ȷ����???????????????????? (����)
A����Ӧ��ǰ50 s ��ƽ������v(PCl3)�� 0.0032 mol��L��1��s��1
B�����������������䣬�����¶ȣ�ƽ��ʱc(PCl3)�� 0.11 mol��L��1����Ӧ�Ħ�H<0
C����ͬ�¶��£���ʼʱ�������г���1.0 mol PCl5��0.20 mol PCl3��0.20 mol Cl2����Ӧ�ﵽƽ��ǰv(��)>v(��)
D����ͬ�¶��£���ʼʱ�������г���2.0 mol PCl3��2.0 mol Cl2���ﵽƽ��ʱ��PCl3��ת���ʴ���80%
�ο��𰸣�D
���������v(PCl3)��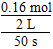 ��0.0016 mol��L��1��s��1��A����������¶�ʱ��c(PCl3)��0.1 mol��L��1��Ϊ0.11 mol��L��1��˵��ƽ�������ƶ�����H>0��B���������ʼʱŨ�������仯��ƽ��ʱv����v�棬C���������ѹǿ��ƽ�������ƶ���PCl3��ת���ʴ���80%��D����ȷ�� ��0.0016 mol��L��1��s��1��A����������¶�ʱ��c(PCl3)��0.1 mol��L��1��Ϊ0.11 mol��L��1��˵��ƽ�������ƶ�����H>0��B���������ʼʱŨ�������仯��ƽ��ʱv����v�棬C���������ѹǿ��ƽ�������ƶ���PCl3��ת���ʴ���80%��D����ȷ��
�����Ѷȣ�һ��
|