微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+
B.Cu溶于稀硝酸HNO3:Cu+2H++NO3-=Cu2++NO2↑+H2O
C.Fe2(SO4)3溶液和Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓
D.向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
2、选择题 下列离子方程式改写成化学方程式正确的是
A.Cu2+ +2OH- =Cu(OH)2 CuCO3+2NaOH=Cu(OH)2+Na2CO3
B.CO32- + 2H+ = CO2 + H2O BaCO3 + 2HCl =BaCl2+ CO2 + H2O
C.Ca2+ + CO32- = CaCO3 Ca(NO3)2+NaCO3 = CaCO3+NaNO3
D.H+ +OH- = H2O 2KOH+H2SO4 = K2SO4 +2H2O
3、选择题 下列反应的离子方程式不正确的是
A.氯化钡和稀硫酸反应:Ba2++SO42- = BaSO4 ↓
B.铁与稀盐酸反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
C.锌与硫酸铜溶液反应:Zn+Cu2+ = Zn2++Cu
D.氢氧化钠和盐酸反应:OH-+ H+ = H2O
4、选择题 下列离子方程式正确的是
A.氯化镁溶液中滴入NaOH溶液:MgCl2 + 2OH―
5、填空题 (14分)钨是我国丰产元素,也是熔点最高的金属,被誉为“光明使者”。用黑钨矿[FeWO4、MnWO4(W为+6价)]结合其它化工生产高纯钨的化工流程如下。已知H2WO4是不溶于水的弱酸,受热可分解生成氧化物。请回答下列有关问题:
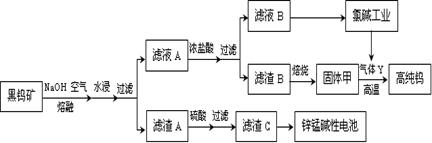
(1)上述流程中通入空气的目的是 ;
(2)滤渣A与硫酸反应的离子方程式为 ;
(3)实验室用锌锰碱性电池作做电源模拟氯碱工业的装置如下图:
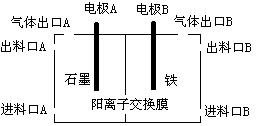
已知:锌锰碱性电池的总反应为Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH,则锌锰碱性电池的锌电极应与装置中电极 (填“A”或“B”)相接,气体Y为气体出口 (填“A”或“B”)出来的气体,为提高生产效率,电解开始时,从进料口B加入的物质为 ,写出锌锰碱性电池正极反应式 ;
(4)已知:单质碳也可与固体甲制得钨,用气体Y而不用单质碳的原因 ;
(5)将H2与CO2以4:1的体积比混合,在适当的条件下可制得CH4。已知:
CH4 (g) + 2O2(g)  CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol
CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol
H2(g) + 1/2O2(g)  H2O(1) ΔH2=-285.8 kJ/mol
H2O(1) ΔH2=-285.8 kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是 。