微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.32 g O2占有的体积约为22.4 L
B.22.4 L N2含阿伏加德罗常数个氮分子
C.在标准状况下,22.4 L水的质量约为18 g
D.22 g CO2与标准状况下的11.2 L HCl含有相同的分子数
参考答案:D
本题解析:
试题分析:1mol O2,在标准状况下占有的体积约为22.4 L,故A项错误;在标准状况下22.4 L N2,含阿伏加德罗常数个氮分子,故B错误;在标准状况下,水是液体,故C错误; 22 g CO2的物质的量为0.5mol,标准状况下的11.2 L HCl的物质的量为0.5mol,故D正确。
考点:本题考查气体摩尔体积。
本题难度:一般
2、选择题 (8分)同温同压下,同体积的H2和CO2物质的量之比为?????,原子个数之比?????,质量比?????;若两者所含原子个数相等,它们的物质的量比是?????????。
参考答案:(8分)1:1 ,2:3 ,
本题解析:略
本题难度:一般
3、计算题 将0.04molKMnO4固体加热,一段时间后,收集到amol气体,此时KMnO4的分解率为x,在反应后的残留固体中加入足量的浓盐酸,又收集到bmol气体(设Mn元素全部以Mn2+存在于溶液中)。试填写:
(1)a+b=__________(用x表示)。
(2)当x=__________时,a+b取最小值,且最小值为___________。
(3)当a+b=0.09时,加热后所得残留固体的质量为___________g。
参考答案:(1)a+b=0.1-0.02x;(2)当x=1,a+b有最
本题解析:利用化学方程式,结合数学知识解决化学问题。
解析:(1)参加分解反应的KMnO4物质的量为0.04xmol,剩余的KMnO4物质的量为0.04(1-x)mol,根据化学方程式计算。
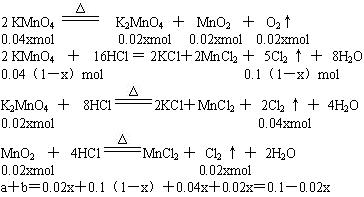
(2)因为x≤1,当x=1,a+b有最小值,最小值为0.08。
(3)当a+b=0.0
本题难度:简单
4、选择题 下列实验操作使测定(或配制)结果偏低的是( )
A.测量一包固体的质量,将药品放在右盘,砝码放在左盘
B.中和滴定用的锥形瓶加入少量待测液润洗后,再加待测液
C.在保温容器中测量NaOH和稀盐酸反应的中和热时加入稍过量的NaOH溶液
D.配制一定物质的量浓度的溶液,定容时仰视刻度线
参考答案:D
本题解析:
本题难度:简单
5、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.在0 ℃时,22.4 L氢气中含有2NA个氢原子
B.电解食盐水若产生2 g氢气,则转移的电子数目为NA
C.1 mol乙烷分子中共价键总数为7NA
D.密闭容器中46 g NO2含有的分子数为NA
参考答案:C
本题解析:A项不是标准 状况下,无法求算,错误;根据2NaCl+2H2O 2NaOH+Cl2↑+H2↑分析可知,若产生2 g H2,即1 mol,需转移电子数为2NA,B项错误;根据乙烷的结构简式为CH3CH3,可知1 mol分子中共价键数为7NA,C项正确;在密闭容器中存在平衡2NO2
2NaOH+Cl2↑+H2↑分析可知,若产生2 g H2,即1 mol,需转移电子数为2NA,B项错误;根据乙烷的结构简式为CH3CH3,可知1 mol分子中共价键数为7NA,C项正确;在密闭容器中存在平衡2NO2 本题难度:一般
本题难度:一般