��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪25�桢101kPa�£�ʯī�����ʯȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ
C(ʯī)+O2(g)=CO2(g) ��H=��393.51kJ��mol-1
C(���ʯ)+O2(g)=CO2(g) ��H=��395.41kJ��mol-1
�ݴ��жϣ�����˵������ȷ���� [???? ]
A����ʯī�Ʊ����ʯ�����ȷ�Ӧ��������ʱ��ʯī�������Ƚ��ʯ�ĵ�
B����ʯī�Ʊ����ʯ�����ȷ�Ӧ��������ʱ��ʯī�������Ƚ��ʯ�ĸߡ�
C����ʯī�Ʊ����ʯ�Ƿ��ȷ�Ӧ��������ʱ��ʯī�������Ƚ��ʯ�ĵ͡�
D����ʯī�Ʊ����ʯ�Ƿ��ȷ�Ӧ��������ʱ��ʯī�������Ƚ��ʯ�ĸ�
2������� ���ý�̿����Ȼ����ȡ���۵�CO��H2�������ڰ��ϳɺ��л��ϳ���Ŀǰ��ҵ��������Ҫ;����
��1����֪��CH4��g��+2O2?��g��=CO2?��g��+2H2O?��l����H=-890.3kJ?mol-1?????��
H2��g��+1/2O2?��g��=H2O?��l����H=-285.8kJ?mol-1?��
CO��g��+1/2O2��g��=CO2��g����H=-283.0kJ?mol-1?��
H2O��g��=H2O��l����H=-44.0kJ?mol-1?��
��ӦCH4��g��+H2O��g��
?����?
.
?
??CO��g��+3H2��g������H=______kJ?mol-1����״����33.6L�����������ˮ������ȫ��Ӧ����CO��H2����Ӧ������ת��______mole-���ų�______kJ������
��2��һ�������£������Ϊ5L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g��+2H2��g��?CH3OH��g������ͬ�¶�ʱ��������ʵ�����ʱ��仯������ͼ��ʾ����������������и��⣺
�ٷ�Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK=______�������¶ȣ�Kֵ______�����������С�����䡱����
����300�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��=______��������ط��ź����ݱ�ʾ��
���жϸÿ��淴Ӧ�ﵽƽ��״̬�ı�־��______��������ĸ��
a��CH3OH������������CO�������������???b�������������ѹǿ����
c�������л��������ܶȱ��ֲ���???????????d��CO�ٷֺ������ֲ���
e��CO��CH3OHŨ�����
�������H2��ת���ʣ����д�ʩ���е���______��������ĸ��
a�����������ٳ���Ar????b���ı䷴Ӧ�Ĵ���
c�����������ٳ���CO??????????????????????d�������¶ȣ�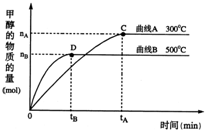
3��ѡ���� 2008��9���ҹ������ߡ��������գ��й�����Աʵ���״�̫�����ߣ����ػ����ԭ�����£�N2H4����Ϊ��������ȼ�ϣ�NO2Ϊ����������Ӧ���ɵ�����ˮ��������֪��
N2(g)+2O2(g)�T2NO2(g)����H=+67.7kJ/mol
N2H4(g)+O2(g)�TN2(g)+2H2O(g)����H=-534kJ/mol
�����ж���ȷ���ǣ� ? ��A���������������������Ļ�ѧ��Ӧ���Ƿ��ȷ�Ӧ
B��N2H4��ȼ����Ϊ534kJ/mol
C������NO2��Ӧ���Ȼ�ѧ����?2N2H4��g��+2NO2��g���T3N2��g��+4H2O��g������H=-1135.7kJ/mol
D��.3.2g����ȫ��Ӧת�Ƶĵ�����Ϊ0.6mol
4��ѡ���� �������ĸ���ѧ��Ӧ���Ȼ�ѧ����ʽ��
��C(s)+O2(g)=CO2(g) ��H1
��2H2(g) +O2(g) =2H2O(l) ��H2
��CH3COOH(l) +2O2(g)=2CO2(g)+2H2O(l) ��H3
��2C(s)+2H2(g)+O2(g)=CH3COOH(l) ��H4
�����ʱ�֮��Ĺ�ϵ��ȷ���� [???? ]
A��2��H1=��H2 - ��H3+��H4
B����H2= 2��H1-��H3+��H4
C����H3=2��H1 +��H2+��H4
D����H4= 2��H1+��H2-��H3
5������� �ؾ�ʯ��BaSO4��������ˮ��Ҫת����BaCO3���Ʊ��������Σ���ҵ��һ����ø������ջ�ԭ����ʵ���ҿ��Բ��ó���ת������
��������ջ�ԭ��
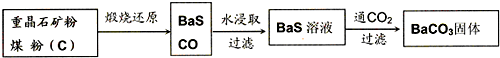
��1�����ջ�ԭ���Ȼ�ѧ����ʽΪ��______
�йص����ݣ�Ba��s��+S��s��+2O2��g��=BaSO4��s������H=-1473.2kJ?mol-1
C��s��+ 1
2
O2��g��=CO��g������H=-110.5kJ?mol-1
Ba��s��+S��s��=BaS��s������H=-460kJ?mol-1
��2��������BaS��ˮ��Һ�ʼ��ԣ�ԭ���ǣ������ӷ���ʽ��ʾ����______��
�����ת����
��BaSO4�����м��뱥��Na2CO3��Һ����ֽ��裬��ȥ�ϲ���Һ����˴�����Σ�ֱ��BaSO4ȫ��ת��ΪBaCO3��BaSO4��s��+CO32-��aq���PBaCO3��s��+SO42-��aq����ƽ�ⳣ��K=0.042��
��3������0.20mol?BaSO4��ÿ����1.00L?2.0mol?L-1����Na2CO3��Һ�������ٶ�BaSO4��ȫ��ת����������Ҫ�������ٴΣ���д��������̣�
��4���ӡ���ɫ��ѧ���Ƕȷ������ñ���Na2CO3��Һ����ת�������ŵ���______��
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772
|