微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 制备氢氧化铁胶体的方法是???????????????????????????????????????????????
????????????????????????????????????,可通过???????????????????来区别溶液和胶体。
参考答案:将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加适量饱和FeCl3
本题解析:略
本题难度:简单
2、实验题 医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:
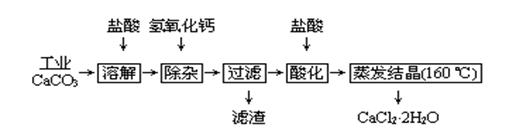
已知:查阅资料得知氢氧化物沉淀时的pH为:
氢氧化物
| Fe(OH)3
| Al(OH)3
|
开始沉淀时的pH
| 2.3
| 4.0
| 开始溶解:7.8
|
完全沉淀时的pH
| 3.7
| 5.2
| 完全溶解:10.8
?
(1)CaCO3与盐酸反应的离子方程式???????????????????????????????????????。
(2)除杂操作是加入氢氧化钙,调节溶液的pH为?????????????????,目的是除去溶液中少量的Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是?????????????????
????????????????????????????????????????????????????????????????。
(3)过滤时需用的玻璃仪器有??????????????。滤渣主要成分的化学式???????????。
(4)酸化时加盐酸的目的为:①??????????????????????????????????,②防止Ca2+ 在蒸发时发生水解。
(5)为什么蒸发结晶要保持在160℃:???????????????????????????????????????。
(6)测定晶体样品的纯度:若用一定浓度的AgNO3溶液滴定一定质量的晶体样品,所测样品中CaCl2 ・2H2O的质量分数偏高(忽略其它实验误差),可能的原因之一为?????????????????????????????????????。
参考答案:(16分,每空2分)
(1)CaCO3+2H+=Ca2
本题解析:
试题分析:(1)盐酸是强酸,酸性比碳酸强,则难溶于水的碳酸钙易溶于盐酸,生成可溶性的氯化钙、二氧化碳气体和水,将易溶且易电离的化合物改写成离子形式,其余物质都保留化学式,删去实际上未反应的离子,则该反应为CaCO3+2H+=Ca2++CO2↑+H2O;(2)根据表中氢氧化物完全沉淀时的pH可知,除去溶液中少量铁离子和铝离子应使溶液pH介于5.2~7.8之间或者5.2≤pH<7.8,低于3.7时铁离子不能完全变为氢氧化铁沉淀,低于5.2时铝离子不能完全变为氢氧化铝沉淀,高于7.8时,氢氧化铝开始变为偏铝酸根离子,溶液又引入新的杂质;检验氢氧化铁是否沉淀的方法就是检验溶液中是否存在铁离子,由于铁离子遇KSCN溶液变红的特征反应,通常设计的实验方案为:静置,取少量上层清液于小试管中,滴加KSCN溶液,若不显红色,则Fe(OH)3沉淀完全,反之,则Fe(OH)3沉淀不完全;(3)过滤属于化学实验基本操作,也是混合物分离与提纯的常用方法,主要使用烧杯、玻璃棒、普通漏斗等仪器;当溶液pH介于5.2~7.8之间时,铁离子、铝离子完全变为氢氧化铁沉淀、氢氧化铝沉淀,则过滤所得滤渣的成分为Fe(OH)3、Al(OH)3;(4)氢氧化钙是除杂试剂,除杂试剂一定过量,氢氧化钙是强碱,由于目标产物是氯化钙,则酸化时加入盐酸的目的是除去过量的氢氧化钙,将其转化为氯化钙,防止氢氧化钙吸收空气中的二氧化碳,且过量的盐酸受热易挥发逸出(逸出的氯化氢气体可循环利用),不能加硝酸或硫酸酸化,因为它们除去旧杂质时会引入硝酸根离子或硫酸根离子等新杂质;(5)结晶水化合物受热可能失去结晶水,蒸发结晶要控制温度在160℃的原因是,温度太高,二水合氯化钙会失去结晶水;(6)滴定原理为:Ag++Cl-=AgCl↓,若氯离子的物质的量偏大,则测定结果偏高;酸化后所得溶液主要含有氯化钙、氯化钠、氯化氢,蒸发结晶时逸出氯化氢,但是没有除去钠离子,则所得晶体是二水合氯化钙和氯化钠的混合物,氯元素的质量分数:CaCl2>NaCl> CaCl2?H2O >CaCl2?2H2O,因此晶体样品中含有NaCl或二水合氯化钙失去全部或部分结晶水得到的CaCl2或CaCl2?H2O,都能导致所含氯元素的质量分数偏高,则所测样品二水合氯化钙的质量分数偏高。
本题难度:困难
3、实验题 现某实验需要480 mL 0.2 mol/L的Na2CO3溶液,现用Na2CO3・10H2O晶体配制该溶液。?
(1)① 实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少??????????????????;
② 实验中两次用到玻璃棒,其作用分别是??????????????、??????????????。
(2) 应称取Na2CO3・10H2O晶体的质量为:?????????????。??
(3)根据下列操作对所配溶液的浓度各有什么影响,将其序号填在下面空格:?
①碳酸钠失去了部分结晶水;????②用“左码右物”的称量方法称量晶体;
③碳酸钠晶体不纯,其中混有氯化钠;?④容量瓶中原有少量蒸馏水。?
⑤定容时俯视液面;?⑥摇匀后发现液面低于刻度线再加水。
其中引起所配溶液浓度:a.偏高的有??????????????????????????????;
b.偏低的有??????????????????????????????;
c.无影响的有????????????????????????????。
参考答案:(1)①500 mL容量瓶、胶头滴管????② 搅拌???引
本题解析:略
本题难度:简单
4、填空题 (每空2分,共12分)实验室欲配制220mL 0.2 mol・L-1的碳酸钠溶液,回答下列问题:
可供选择的仪器:①量筒②胶头滴管③托盘天平④药匙⑤烧瓶⑥烧杯
(1)通过计算可知,应用托盘天平称取??????????????????????g碳酸钠晶体(Na2CO3?10H2O)
(2)配制过程需要的仪器______________(填序号),还缺少的仪器有????????????
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次)_____________;
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.用托盘天平准确称取所需的Na2CO3固体的质量,放入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作_____________;若定容时俯视刻度线______________。
参考答案:(每空2分,共12分)(1) 14.3???????? (2
本题解析:考查一定物质的量浓度溶液的配制
(1)由于没有220ml规格的容量瓶,所以应该配制250ml的,即溶质的物质的量是0.25L×0.2mol/L=0.05mol,所以需要Na2CO3?10H2O的质量是0.05mol×286g/mol=14.3g。
(2)根据配制过程可判断,需要的仪器是②③④⑥。还缺少250ml容量瓶、玻璃棒。
(3)根据配制过程可知,正确的操作顺序是BCAFED。
(4)如果没有洗涤,则溶质的物质的量偏小,测定结果偏低;定容时俯视刻度线,则容量瓶中溶液的体积偏小,测定结果偏高。
本题难度:简单
5、选择题 某学习小组拟利用如下装置制备氮化钙(化学式:Ca3N2, 极易与H2O反应),下列说法正确的是
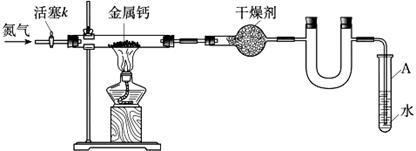
A.打开活塞K通入N2,试管A内有气泡产生,说明装置气密性良好
B.U形管中盛放的干燥剂既可以用碱 石灰,也可以用浓硫酸 石灰,也可以用浓硫酸
C.反应结束后,先熄灭酒精灯,待反应管冷却后再关闭活塞K
D.将产物Ca3N2放入盐酸中,只能得到一种盐
参考答案:C
本题解析:略
本题难度:一般
|