微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 过碳酸钠(Na2CO3・3H2O2),有固体双氧水的俗称,该晶体具有Na2CO3和H2O2的双重性质,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中,过碳酸钠的某生产流程如下图所示。
已知:2Na2CO3+3H2O2=2Na2CO3・3H2O?△H<0;回答下列问题:

(1)下列物质可使过碳酸钠较快失效的是(填序号)_________。
A.FeCl3溶液
B.H2S
C.稀硫酸
D.NaHCO3溶液
(2)反应①应先通入的气体是__________。
(3)在上述流程中,向反应前的H2O2中加入稳定剂的作用是____________________。
(4)该生产流程中可循环使用的物质是______________________________(填化学式)。
(5)生产过碳酸钠的流程中遗漏了一步,造成所得产品纯度偏低,请简述该步操作过程___________。
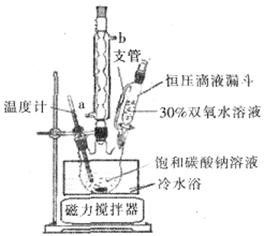
(6)实验室利用下图装置制备过碳酸钠,该装置中恒压滴液漏斗中支管的作用是_______,冷凝管应从__________处进水。
(7)由实验测定反应温度对产物的影响如下表:根据下表数据,你认为反应最佳的温度选择的范围是_______________。
T/℃
| 活性氧百分含量
| 产率
|
5~10
| 13.94
| 85.49
|
10~15
| 14.02
| 85.78
|
15~20
| 15.05
| 88.38
|
20~25
| 14.46
| 83.01
 、 、
参考答案:(1)ABC(3分) (2)NH3(2分) (3)防止双氧水
本题解析:
试题分析:(1)过碳酸钠(Na2CO3・3H2O2)具有Na2CO3和H2O2的双重性质,则A、FeCl3溶液能与碳酸钠反应,因此氯化铁也与过碳酸钠反应,A正确;B.H2S与双氧水发生氧化还原反应,则也与过碳酸钠发生氧化还原反应,B正确;C.稀硫酸与碳酸钠反应,因此也与过碳酸钠反应,C正确;D.NaHCO3溶液与碳酸钠以及双氧水等均不反应,因此也与过碳酸钠不反应,D不正确,答案选ABC。
(2)二氧化碳在水中的溶解度很小,而氨气极易溶于水,所以反应①应先通入的气体是氨气。
(3)由于双氧水稳定性差,易分解,因此向反应前的H2O2中加入稳定剂的作用是防止双氧水分解。
(4)碳酸氢钠分解生成碳酸钠、水和二氧化碳,即A是碳酸钠,B是二氧化碳,因此该生产流程中可循环使用的物质是CO2。
(5)从溶液中过滤出固体后,需要洗涤沉淀,因此该步操作是沿玻璃棒向漏斗(过滤器)中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复操作数次。
(6)恒压滴液漏斗能保持压强恒定,因此恒压滴液漏斗中支管的作用是使液体顺利流下。冷凝管应从下端进水,即a处进水上端出水。
(7)根据下表数据可知温度超过20℃后,活性氧百分含量和产率均降低,所以反应最佳的温度选择的范围是15~20℃。
本题难度:一般
2、实验题 下列实验方案正确且能达到相应实验预期目的的是

| 
| 
| 
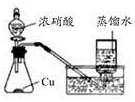
| A.制取少量蒸馏水
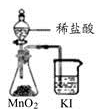
| B.制取少量NO2
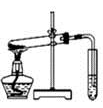
| C.比较MnO2、Cl2、I2的氧化性
| D.探究NH4HCO3的热稳定性
?
参考答案:A
本题解析:A装置可以蒸出蒸馏水,A项正确。B装置NO2不能用排水法收集,B项错误。C装置中用稀盐酸制氯气错误,C项错误。NH4HCO3受热分解产生水,被加热的试管口应向下倾,D项错误。
本题难度:一般
3、选择题 用NaCl固体配制0.1 mol・L-1的NaCl溶液,下列操作或说法正确的是(???)
A.将5.85gNaCl固体溶于1 L水中可配成0.1 mol・L-1的NaCl溶液
B.定容时仰视观察液面,实验结果偏低
C.固体溶解后,将溶液转移到容量瓶中,然后向容量瓶中直接加水稀释到刻度线
D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
参考答案:BD
本题解析:
试题分析:A项:1 L水的体积并不是溶液的体积,溶液体积大于水的体积,配制溶液的溶度会小,故错;C项:将溶液转移到容量瓶中,要左右震荡容量瓶,故错。故选BD。
点评:本题考查的是溶液的配制。学生要掌握住其步骤,才能正确的解答此类问题。
(1)计算:计算配制所需固体溶质的质量或液体浓溶液的体积。
(2)称量:用托盘天平称量固体质量或用量筒(应用移液管,但中学阶段一般用量筒)量取液体体积。
(3)溶解:在烧杯中溶解或稀释溶质,恢复至室温(如不能完全溶解可适当加热)。检查容量瓶是否漏水
(4)转移:将烧杯内冷却后的溶液沿玻璃棒小心转入一定体积的容量瓶中(玻璃棒下端应靠在容量瓶刻度线以下)。
(5)洗涤:用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转入容器中,振荡,使溶液混合均匀。
(6)定容:向容量瓶中加水至刻度线以下1cm~2cm处时,改用胶头滴管加水,使溶液凹面恰好与刻度线相切。
(7)摇匀:盖好瓶塞,用食指顶住瓶塞,另一只手的手指托住瓶底,反复上下颠倒,使溶液混合均匀。
最后将配制好的溶液倒入试剂瓶中,贴好标签。
影响:
1.称量时引起误差。
2.未将烧杯洗涤,使溶液的物质量减少,导致溶液浓度降低。
3.转移时不小心溅出溶液,导致浓度偏低。
安全注意:
1.氢氧化钠为碱性化学物质,浓盐酸为酸性化学物质,注意不要溅到手上、身上、以免腐蚀!
2.要注意计算的准确性
3.注意移液管的使用
4.稀释浓硫酸是把酸加入水中,用玻璃棒搅拌。
5.容量瓶在使用前必须检漏,检漏的步骤为注入自来水至标线附近,盖好瓶塞.右手托住瓶底,倒立2min,观察瓶塞是否渗水。如不漏,将塞子旋转180度,再检漏.如漏水,需换一套容量瓶,再检漏。
6.在配置由浓液体稀释而来的溶液时,如由浓硫酸配置稀硫酸时,不应该洗涤用来称量浓硫酸的量筒,因为量筒在设计的时候已经考虑到了有剩余液体的现象,以免造成溶液物质的量的大小发生变化!
7.移液前应静置至溶液温度恢复到室温(如氢氧化钠固体溶于水放热,浓硫酸稀释放热,硝酸铵固体溶于水吸热),以免造成容量瓶的热胀冷缩!
本题难度:简单
4、选择题 下列配制银氨溶液的操作中,正确的是(?????? )
A.在洁净的试管中加入1~2mLAgNO3溶液,再加入过量浓氨水振荡混合
B.在洁净的试管中加入1~2mL浓氨水,再加入AgNO3溶液至过量
C.在洁净的试管中加入1~2mL稀氨水,再逐滴加入2% AgNO3溶液至过量
D.在洁净的试管中加入2% AgNO3溶液1~2mL,逐滴加入2%稀氨水至沉淀恰好溶解为止
参考答案:D
本题解析:略
本题难度:简单
5、选择题 检验Cl2是否充满了集气瓶的正确操作为 [???? ]
A.用玻璃棒粘上湿润的碘化钾淀粉试纸伸到集气瓶口附近,观察试纸是否变蓝
B.将AgNO3溶液滴入集气瓶中.观察有无白色沉淀生成
C.用玻璃棒蘸取少许NaOH溶液放人集气瓶口附近,看是否反应
D.用手将湿润的碘化钾淀粉试纸放在集气瓶口上方,观察颜色是否变蓝
参考答案:A
本题解析:
本题难度:简单
|
|