微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知 、
、 、
、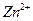 较完全地形成氢氧化物沉淀,溶液的pH分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量
较完全地形成氢氧化物沉淀,溶液的pH分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量 、
、 杂质离子,为除去这些离子制得纯净的硫酸锌,应加入的试剂是:
杂质离子,为除去这些离子制得纯净的硫酸锌,应加入的试剂是:
A. 溶液
溶液
B. 、
、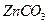
C.氨水
D. 、
、
参考答案:D
本题解析:略
本题难度:简单
2、选择题 某溶液含有Ⅲ中的离子(见下表),欲用Ⅰ中的试剂来检验溶液是否还含有Ⅱ中的离子,能够成功检验的是(说明:在实验过程中不允许加热、过滤、萃取等操作)(???)

参考答案:D
本题解析:
试题分析:A选项稀氨水与Al3+、Mg2+反应都生成白色沉淀,错误。B选项AgCl和AgI沉淀都有颜色,不能有效区别检验,错误。C选项KSCN和Fe3+反应生成红色溶液,不能用于检验Fe2+,错误。D选项正确BaSO4白色沉淀不溶解于酸,正确。
本题难度:一般
3、选择题 下列叙述正确的是
A.标准状况下,1 mol物质的体积约为22.4 L
B.标准状况下,28 g一氧化碳与氮气的混合气的体积约为22.4 L
C.22.4 L氢气与44.8 L氦气所含的原子数相等
D.1 molH2O(g)在标准状况下的体积约为22.4 L
参考答案:B
本题解析:正确解法:物质的状态包括气态、固态和液态,气体摩尔体积的研究对象是气体物质,而非所有物质,A选项错误;CO和N2的摩尔质量相等,都是28 g/mol,所以混合气体的物质的量为1 mol,故二者的混合气在标准状况
下的体积约为22.4 L,B选项正确;C选项中没有标明温度和压强,无法得知各气体的物质的量,因而不能确定它们的原子数是否相等,该选项的说法是错误的;D选项中虽然给的是水蒸气,但在标准状况下水是以冰水混合物的形式存在,题中说法有误,1 molH2O(g)在标准状况下的体积小于22.4 L.
点评:质量和物质的量不受外界条件的影响,但气体的体积受外界条件的影响;气体摩尔体积针对的是气体,“22.4 L/mol”是在0℃、101 kPa(标准状况)时的气体摩尔体积,在非标准状况下,1 mol气体的体积不一定是22.4 L.
本题难度:困难
4、填空题 (12分) 有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子:(每种物质只含一种阳离子和一种阴离子且互不重复)
阳离子
| Na+、Ba2+、NH4+、K+
|
阴离子
| CH3COO-、Cl-、OH-、SO42-
?
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B溶液中水的电离程度相同;D溶液焰色反应显黄色。
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成有刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A的名称是____________。
(2)用离子方程式表示A的水溶液显碱性的原因______________________________。
(3)25 ℃时pH=9的A溶液和pH=9的C溶液中水的电离程度较小的是________(填写A或C的化学式)。
(4)25 ℃时用惰性电极电解D的水溶液,一段时间后溶液的pH________7(填“>”、“<”或“=”)。
(5)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为__________________________________________________。
(6)室温时在一定体积0.2 mol・L-1的C溶液中,加入一定体积的0.1 mol・L-1的盐酸时,混合溶液的pH=13,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是________。
参考答案:(12分)(1)醋酸钾????(2)CH3COO-+H2O<
本题解析:
试题分析:(1)D溶液焰色反应显黄色,说明含有Na+。C溶液和D溶液相遇时只生成白色沉淀,则白色沉淀是硫酸钡,因此D是硫酸钠。B溶液和C溶液相遇时只生成有刺激性气味的气体,则该气体是氨气。又因为A、C溶液的pH均大于7,B溶液的pH小于7,所以B是氯化铵,则C氢氧化钡,A就是醋酸钾。
(2)醋酸钾是强酸弱碱盐,水解显碱性,即CH3COO-+H2O CH3COOH+OH-。 CH3COOH+OH-。
(3)醋酸钾水解促进水的电离,氢氧化钡是强碱,抑制水的电离,所以溶液中水的电离程度较小的是Ba(OH)2。
(4)惰性电极电解硫酸钠溶液,则实质是电解水,溶液始终显中性,即pH=7。
(5)等体积、等物质的量浓度的B溶液和C溶液混合后,氢氧化钡过量,因此反应后溶液中各种离子浓度由大到小的顺序为c(OH-)>c(Ba2+)=c(Cl-)>c(NH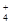 )>c(H+)或c(OH-)>c(Cl-)=c(Ba2+)>c(NH )>c(H+)或c(OH-)>c(Cl-)=c(Ba2+)>c(NH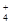 )>c(H+)。 )>c(H+)。
(6)混合溶液的pH=13,即OH-的浓度是0.1mol/L。这说明氢氧化钡是过量的,则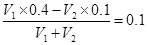 ,解得 ,解得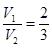 。 。
点评:该题是高考中的常见题型,属于中等难度的试题,试题基础性强,难易适中、注重考查学生分析问题、以及灵活运用基础知识解决问题的能力。有助于培养学生的逻辑思维能力和发散思维能力,提高学生的应试能力和学习效率。
本题难度:一般
5、选择题 30 mL 1 mol/L NaCl溶液和40 mL 0.5 mol/L CaCl2溶液混合之后(体积的变化忽略不计),混合液中Cl-的物质的量浓度为??????????????????
A.0.5 mol/L
B.0.6 mol/L
C.1 mol/L
D.2 mol/L
参考答案:C
本题解析:试题分析:根据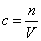 可知,混合后溶液中氯离子的浓度是 可知,混合后溶液中氯离子的浓度是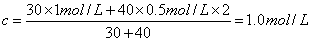 ,答案选C。 ,答案选C。
考点:考查溶液中离子浓度的有关计算
点评:该题是高考中的常见题型,属于基础性试题的考查。该题的关键是明确溶液中氯离子的来源,然后结合公式直接列式计算即可,有助于培养学生的应试能力。
本题难度:一般
|