原理
A
分离溶于水中的碘
乙醇萃取
碘在乙醇中的溶解度较大
B
分离乙酸乙酯和乙醇
分液
乙酸乙酯和乙醇的密度不同
C
除去KNO3固体中混杂的NaCl
重结晶
NaCl在水中的溶解度很大
D
除去丁醇中的乙醚
蒸馏
丁醇与乙醚的沸点相差较大
A.A
B.B
C.C
D.D
参考答案:A.乙醇和水混溶,不能用作萃取剂,应用四氯化碳或苯萃取,故A
本题解析:
本题难度:一般
2、实验题 Ⅰ:选择一种试剂鉴别下列各组物质,将所选试剂的化学式或名称写在横线上:
① 苯、甲苯??????????② 苯、硝基苯、乙醇???????
③ 苯酚溶液、己烯、己烷、醋酸溶液?????????????
Ⅱ:为了探究苯酚和乙醇分子中羟基上氢原子的活泼性,甲、乙两位同学分别设计如下甲、乙两方案。
方案甲:
实验1:取少量无水乙醚于试管中,加入少量金属钠。
实验2:各取3mL无水乙醚于试管中,分别加入少量等物质的量的苯酚和乙醇,再投入大小相同的钠块。
方案乙:
各取少量等物质的苯酚和乙醇于试管中,均在60℃的水浴加热,待苯酚熔化后,各放入相同大小的一小块金属钠。(已知:苯酚的密度为1.07g/mL)
(1)方案甲设计实验1的目的是??????????????????????????????。
(2)方案乙中观察到:在乙醇中,钠很快与乙醇反应产生气体,溶液保持澄清;在苯酚中,钠块表面有少量气泡,且表面产生白色悬浮物,最后白色悬浮物充满苯酚熔融液。
①实验中观察到的白色悬浮物为???????????;
②苯酚熔融液与钠的反应速率不如无水乙醇与钠的反应快,其可能原因有____________、_____________。
参考答案:I:①酸性KMnO4溶液、②水、③溴水 (其它合理答案也给分
本题解析:
试题分析:Ⅰ①苯、甲苯可以用酸性KMnO4溶液来鉴别,因为甲苯能够被酸性KMnO4溶液从而使其褪色,而苯不能;②苯、硝基苯、乙醇可以用水来鉴别,乙醇可以和水互溶,而苯、硝基苯与水不互溶,苯的密度比水小,在上层,而硝基苯的密度比水大,在下层;③苯酚溶液、己烯、己烷、醋酸溶液可以用溴水来鉴别,苯酚与溴水反应生成了白色沉淀,己稀能够使溴水褪色,己烷与溴水发生了萃取作用,上层为红色,醋酸与溴水互溶;
Ⅱ取少量无水乙醚于试管中,加入少量金属钠的目的是证明 钠与乙醚不反应,烃基上的氢不能被钠取代;①苯酚与钠反应得到苯酚钠和氢气,所以实验中观察到的白色悬浮物为苯酚钠;②苯酚熔融液与钠的反应速率不如无水乙醇与钠的反应快,其可能原因有反应物接触面积小,生成的苯酚钠将钠包起来,阻止了反应的进行。
点评:本题考查了物质的鉴别、探究性实验,这种题型是高考的常见题型,本题有利于提高学生的探究性思维,本题难度适中。
本题难度:简单
3、简答题 工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
请回答下列问题:
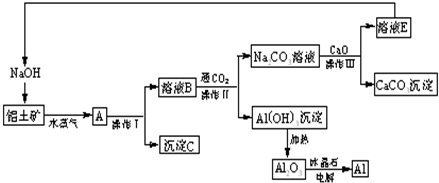
(1)操作I、操作II、操作III 都是______(填操作名称),实验室要洗涤Al(OH)3沉淀应该在______装置中进行.
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有______(填化学式).用此法制取铝得到的副产品是______(填化学式).
(3)写出Na2CO3溶液与CaO反应离子方程式:______.
(4)若铝土矿中还含有二氧化硅,此生产过程中得到的氧化铝将混有杂质:______(填化学式).
参考答案:(1)实现固体和液体的分离采用过滤法,实验室要洗涤Al(OH
本题解析:
本题难度:一般
4、选择题 下列关于某溶液所含离子检验的方法和结论正确的是
A.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+
B.通入少量Cl2后,溶液变为黄色,再加入淀粉溶液后,溶液变蓝,说明有I-
C.加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中一定有CO32-或SO32-
D.往溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成,说明一定有SO42-
参考答案:B
本题解析:略
本题难度:简单
5、选择题 将物质的量浓度为a mol/L的酒精溶液和3a mol/L的酒精溶液等质量混合(假设混合溶液的体积等于两溶液的体积之和),则混合后溶液的物质的量浓度
A.=2a mol/L
B.>2a mol/L
C.<2a mol/L
D.不确定
参考答案:B
本题解析:
本题难度:困难
|