微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 氨的接触催化氧化反应4NH3(g) +5O2(g)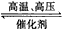 4NO(g)+6H2O(g) △H=-1025 kJ/mol是工业上制备硝酸的重要反应。一定条件下将4 mol NH3和5 mol O2混合于固定容积为2L的密闭容器中,经10s该反应达平衡,并测得NO的浓度为0.8 mol/L。下列判断正确的是 [???? ]
4NO(g)+6H2O(g) △H=-1025 kJ/mol是工业上制备硝酸的重要反应。一定条件下将4 mol NH3和5 mol O2混合于固定容积为2L的密闭容器中,经10s该反应达平衡,并测得NO的浓度为0.8 mol/L。下列判断正确的是 [???? ]
A.达平衡时,2v正(NH3)=3v逆(H2O)
B.反应达到平衡状态时NH3的转化率为20%
C.升高温度能使 减小
减小
D.将容器的体积变为4L,平衡时NO的浓度小于0.4 mol/L
参考答案:C
本题解析:
本题难度:一般
2、选择题 在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)  ?C(g)+D(g)已达到平衡状态???
?C(g)+D(g)已达到平衡状态???
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平均相对分子质量 ⑥v(C)与v(D)的比值 ⑦混合气体的总质量 ⑧混合气体的总体积 ⑨C、D的分子数之比为1∶1
A.①②③④⑤⑥⑦⑧???????????????????B.①③④⑤
C.①②③④⑤⑦ ???????????????????D.①③④⑤⑧⑨
参考答案:B
本题解析:要理解化学平衡状态的特点“等、动、定”的含义,在判断化学平衡状态时还要注意反应前后气体体积是否相等。题给反应是一个反应前后气体体积不相等的反应,因此在定容容器中,若①混合气体的压强、③B的物质的量浓度、④混合气体的总物质的量、⑤混合气体的平均相对分子质量不再变化,均能证明该反应达到化学平衡状态。而②中ρ=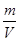 始终不变化,⑥中没指明反应进行的方向,⑦m(g)始终不变化,⑧在定容容器中,混合气体的总体积不能作为判断依据,⑨反应未达到平衡状态时,C、D气体的分子数之比也可能为1∶1。
始终不变化,⑥中没指明反应进行的方向,⑦m(g)始终不变化,⑧在定容容器中,混合气体的总体积不能作为判断依据,⑨反应未达到平衡状态时,C、D气体的分子数之比也可能为1∶1。
本题难度:一般
3、选择题 在一定条件下,某密闭容器中发生如下可逆反应:2SO2(g)+O2(g)==2SO3(g)+Q;达到化学平衡时,SO2、O2和SO3的物质的量之比3:2:4。其它条件不变,升高温度达到新的化学平衡时,二氧化硫为1.4mol,O2为0.9mol,则此时SO3的物质的量为(??? )
A.1.4mol
B.1.6mol
C.1.8mol
D.2.0mol
参考答案:A
本题解析:升高温度平衡向吸热反应方向即逆向移动
_?????? 2SO2??????+????? O2????==?? 2SO3
平1n:???
△n:???? 2n?????????????? n????????? 2n
平2n:?? 1.4mol???????? 0.9mol
所以: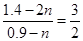 ,可求出n=0.1。则原先平衡时SO2为1.2mol,SO3为1.6mol,新平衡时SO3为1.4mol
,可求出n=0.1。则原先平衡时SO2为1.2mol,SO3为1.6mol,新平衡时SO3为1.4mol
本题难度:一般
4、填空题 (12分)已知下列反应:
①?N2(g)+3H2(g) 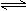 ?2NH3(g);ΔH=-92.4 kJ・mol-1。
?2NH3(g);ΔH=-92.4 kJ・mol-1。
②? 4NH3(g)+5O2(g)=====4NO(g)+6H2O(g);ΔH<0
(1)在500℃、2.02×107Pa和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是______________________________????????????____;
(2)为有效提高氢气的转化率,理论上可采取的措施有__________;
A.降低温度
B.最适合催化剂活性的适当高温
C.增大压强
D.降低压强
E.循环利用和不断补充氮气?????? F.及时移出氨
(3)反应②的化学平衡常数表达式K=________________________,
温度降低时,K值______________(填“增大”、“减小”或“无影响” );
);
(4)在0.5L的密闭容器中,加入2.5mol N2和 7.5mol H2,当该反应达到平衡时,测出平衡混合气的总物质的量为6 mol,则平衡时氮气的转化率=??????? ????
????
参考答案:(1)?? <??可逆反应不能进行到底????????
本题解析:略
本题难度:一般
5、选择题 在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)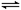 xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol・L-1。下列判断正确的是
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol・L-1。下列判断正确的是
A.A的转化率为40%
B.2 min内B的反应速率为0.2 mol・(L・min)-1
C.x=2
D.若混合气体的密度不变,则表明该反应已达到平衡状态
参考答案:A
本题解析:生成0.8 mol D,则消耗A是1.2mol,所以A的转化率是1.2÷3×100%=40&,A正确。消耗B是0.4mol,所以B物质反应速率是0.4mol÷2L÷2min=0.1mol・(L・min)-1,B不正确。C的浓度为0.2 mol・L-1,则生成C是0.2 mol・L-1×2L=0.4mol,所以根据变化量之比是相应的化学计量数之比可知,x=1,C不正确。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,D不正确。答案选A。
本题难度:简单