微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中,不属于电解质的是
A.Fe
B.NaCl
C.NaOH
D.H2SO4
参考答案:A
本题解析:分析:电解质是在熔融状态或水溶液中能导电的化合物,单质、混合物既不是电解质也不是非电解质.
解答:A、Fe属于单质,既不是电解质也不是非电解质,故A选;
B、NaCl属于盐,在熔融状态或水溶液中能导电,属于电解质,故B不选;
C、NaOH属于碱,在熔融状态或水溶液中能导电,属于电解质,故C不选;
D、H2SO4属于酸,在水溶液中能导电,属于电解质,故D不选.
故选A.
点评:本题考查电解质、非电解质的概念,题目难度不大,注意电解质和非电解质都属于化合物.
本题难度:简单
2、选择题 当碳、氢、氧、氮、溴等元素的原子量均取整数时,下列说法正确的是
A.a一氨基酸的式量均为偶数;
B.硝基化合物的式量均为奇数
C.烃及烃的含氧衍生物的式量均为偶数
D.溴代烃的式量均为偶数
参考答案:C
本题解析:
本题难度:简单
3、选择题 下列说法正确的是
A.在化学反应中某元素由化合态变为游离态,该元素一定是被还原
B.失电子难的原子获得电子的能力一定强
C.电子层结构相同的各种离子,它的半径随核电荷数的增加而减少
D.最外层电子数少的金属元素,一定比最外层电子数较它多的金属元素活泼性较强
参考答案:C
本题解析:选项A不正确。在化学反应中,若元素以阳离子或正价形式存在变为中性原子(游离态)时,是被还原了。但若元素以阴离子形式存在转变为中性原子时,则该元素却是被氧化了。例如:

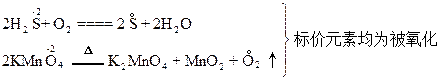
选项B不正确。失电子难的原子,在多数情况下变成离子后得电子就容易些,例如Cu比Zn难失电子,则Cu2+比Zn2+来源:91考试 网易得电子;失电子难的非金属原子,一般地说,其原子得电子就较容易些,如F比Cl难失电子,则F比Cl易得电子。但若对稀有气体来说,由于其原子的最外层已达到8个电子的稳定结构,所以它既不易得电子,也不易失去电子。故选项B未必正确。
选项C正确。“电子层结构相同”是指电子层数和各层电子数均相同,所以此时离子的半径只取决于核电荷数的多少,核电荷数越多,即核所带的正电荷越多,对核外电子的吸引力越强,所以半径越小。故选项C一定正确。
选项D未必正确。对于金属元素而言,它的活泼性强弱主要取决于元素原子失电子能力的大小,而金属原子失电子能力的大小,除了跟最外层电子数多少有关外(一般来说,最外层电子数越少,越容易失电子),还跟金属原子核外电子层结构有关,即与电子层数也有关。层数越多,一般失电子能力越强。所以D未必正确。
本题难度:简单
4、选择题 下列状态的物质,既属于电解质又能导电的是
A.酒精
B.氯化钾晶体
C.液态的氯气
D.熔融的氢氧化钠
参考答案:D
本题解析:电解质必定属于化合物,排除C(液氯为单质);导电必须有自由电子或自由移动的离子,排除A(非电解质)、B(无自由移动离子),答案为D
本题难度:困难
5、选择题 下列四种微粒中,半径由大到小顺序排列的是??
①X? 1s22s22p63s23p4
②Y? 1s22s22p63s23p5
③Z2- 1s22s22p63s23p6
④W? 1s22s22p5
A.①>②>③>④
B.③>④>①>②
C.③>①>②>④
D.①>②>④>③
参考答案:C
本题解析:考查电子排布及元素周期律
四种元素分别为①X:S;②Y:Cl;③Z:Ar;④W:F,而原子半径决定于电子层数及核电荷数:层数越大半径越大,层数相同时,核电荷数越大,半径越小,O族元素的半径远大于相邻元素半径,故四种微粒半径由大到小的顺序排列为:③>①>②>④,选C
本题难度:简单