微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.胶体区别于其他分散系的本质特征是分散质微粒直径在1 nm~100 nm之间
B.NH3的沸点高于PH3,是因为N-H键能大于P-H键能
C.金属阳离子只存在于离子晶体中
D.由非金属元素组成的化合物一定是共价化合物
参考答案:A
本题解析:B不正确,是由于氨气中存在氢键导致的;C不正确,在金属晶体中也存在金属阳离子;D不正确,例如氯化铵等,因此正确的答案选A。
本题难度:一般
2、填空题 (13分)(1)A、B、D为短周期元素,请根据信息回答问题:
元素
| A
| B
| D
|
性质或结构信息
| 工业上通过分离液态空气获得其单质,单质能助燃
| 气态氢化物的水溶液显碱性
| 原子有三个电子层,简单离子在本周期中半径最小
①第一电离能:A?????B(填“>”、“=”、“<”),基态D原子的电子排布式为?????????。
②B和D由共价键形成的某化合物BD在2200℃开始分解,BD的晶体类型为????????????????。
(2)发展煤的液化技术被纳入“十二五规划”,中科院山西煤化所关于煤液化技术的高效催化剂研发项目取得积极进展。已知:煤可以先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇(CH3OH),从而实现液化。
①某含铜离子的离子结构如右图所示:
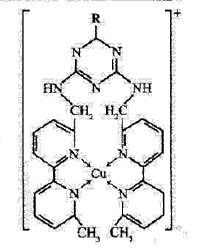
在该离子内部微粒间作用力的类型有:?????????(填字母)。
A.离子键? B.极性键 C.非极性键? D.配位键? E.范德华力? F.氢键
②煤液化获得甲醇,再经催化得到重要工业原料甲醛(HCHO),甲醇的沸点为65℃,甲醛的沸点为-21℃,两者均易溶于水。甲醇的沸点比甲醛高是因为甲醇分子间存在着氢键,而甲醛分子间没有氢键。甲醇和甲醛均溶于水,是因为它们均可以和水形成分子间氢键。请你说明甲醛分子间没有氢键的原因是?????????????????????????????????????????????????。
③甲醇分子中,进行sp3杂化的原子有????????,甲醛与H2发生加成反应,当生成1mol甲醇时,断裂的∏键的数目为????????????
参考答案:(1)① < (1分) ,1s22s22p63s23p
本题解析:(1)空气中能助燃的是氧气,因此A是O。氢化物水溶液显碱性的是氨气,则B是N。D有3个电子层,属于第三周期,离子半径最小,属于D是Al。氮原子的2p轨道是半充满的,稳定性强,所以第一电离能大于氧原子的。铝的原子序数是13,根据构造原理可知基态电子的排布式为1s22s22p63s23p1。AlN的熔点很高,且是由共价键构成的,因此属于原子晶体。
(2)根据结构示意图可判断,氮和氮之间、碳和碳之间形成非极性键,氮和碳之间形成极性键。又因为氮原子含有孤电子对,可以和铜形成配位键。同时氮原子也可以和氢原子形
本题难度:一般
3、选择题 下列变化过程中无化学键断裂或生成的是???????????????????????????????[???? ]
A.石墨转化为金刚石
B.NaCl晶体溶于水
C.干冰升华
D.氮的固定
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列叙述中正确的是(? )
A.主族元素的原子核外电子最后填入的能级是d能级或f能级
B.镁型和铜型金属晶体的配位数均为12
C.中心原子上的孤电子对不参与决定分子的空间结构
D.分子中键角越大,价电子对相互排斥力越大,分子越稳定
参考答案:B
本题解析:
试题分析:A.主族元素的原子核外电子最后填入的能级是s能级或p能级.错误。B.镁型金属是六方最密堆积;铜型金属晶体是面心立方堆积,它们的配位数均为12 。正确。C.如在NH3中的中心原子N杂化方式为sp3,在N原子上有一对孤电子对,它对氨分子中的其它共价键产生排斥力,使分子呈三棱锥型。而CH4中的中心原子C杂化方式也为sp3,在C原子上没有孤电子对,分子呈正四面体型。由此可见孤电子对参与决定分子的空间结构。错误。D.分子中键角越大,价电子对相互排斥力越小,分子越稳定。错误。
本题难度:一般
5、选择题 下列化合物中含有离子键的是( )
A.CO2
B.H3PO4
C.CH3COOH
D.NaCl
参考答案:A.二氧化碳中只含共价键,故A错误;
B.磷酸中只含共
本题解析:
本题难度:简单
|