��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
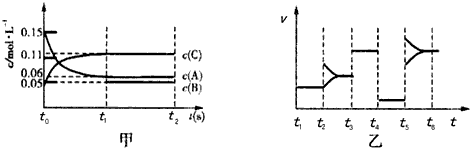
1��ѡ���� ij�ܱ������м���0.3 mol A��0.1 mol C��һ������B�������塣һ�������·�����Ӧ�������ʵ�Ũ����ʱ��仯��ͼ����ʾ[t0~t1��c(B)δ����]��ͼ��Ϊt2��ı以����ͬ��ijһ������Ӧ������ʱ��仯�Ĺ� ϵͼ��t3~t4��ʹ���˴���������˵���������
 [???? ]
[???? ]
A����t1=15s��������C��t0~t1ʱ��ε�ƽ����Ӧ����Ϊ0.004 mol��L-1��s-1
B��t4~t5�θı������Ϊ��Сѹǿ��t5~t6�θı������������ѧ��Ӧ���¶�
C��B����ʼ���ʵ���Ϊ0.02 mol
D���û�ѧ��Ӧ�ı���ʽΪ��3A(g) B(g)+2C(g)
B(g)+2C(g)
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� Ϊ���ٺ�����CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о����״���һ�ֿ�����ȼ�ϣ����ķе�Ϊ64.7�档�п�ѧ�������ɫ���룺�Ѻ���CO2�Ŀ�����ҵβ��ͨ��̼�����Һ�У�Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��õ��״����乹���������£�(���ԭ��������C-12??O-16???Ca-40???Ba-137)

�Իش��������⣺
��1��д���ֽ���з�����Ӧ�Ļ�ѧ����ʽ_________________________��?
��2����2��105Pa��300��ϳ����У�����CO2��H2��Ӧ����32g�״���ˮ���ų�49.5kJ����������д���ϳ����з�����Ӧ���Ȼ�ѧ����ʽ�� ______________________��?
��3���ںϳ����з������Ƿ��ȷ�Ӧ�����²����ڼ״������ɣ��ϳ�����ά��300��Ľϸ��¶ȵ�ԭ�������_______________����Ҫ��״��IJ��ʣ��ɲ�ȡ�Ĵ�ʩ��(д2��)��________________?��______________��
��4���״���һ����Ҫ��������ȼ�ϵ�أ�����KOH���������Һ�������ĵ缫��ӦʽΪ��_____________________��
��5�����³�ѹ�£�����CO2ˮ��Һ�ĵ�pH=5.6��c?(H2CO3)=?1.5��10�C5mol/L��������ˮ�ĵ����H2CO3�Ķ������룬��H2CO3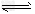 HCO3�C+?H+��ƽ�ⳣ��K=?_________??(����������2λ��Ч���֣���֪10�C5.6=2.5��10�C6)��?
HCO3�C+?H+��ƽ�ⳣ��K=?_________??(����������2λ��Ч���֣���֪10�C5.6=2.5��10�C6)��?
��6��ijͬѧ���ó������ⶨ������CO2����������������CaCO3��BaCO3���ܶȻ������ֱ�Ϊ4.96��10�C9��2.58��10�C9����ͬѧӦ��ѡ�ýϺ��ʵ��Լ���_________(����ĸ)��
A��Ba(OH)2��Һ?????????????????
B��Ca(OH)2��Һ?
C��BaCl2��NaOH�����Һ???????
D��CaCl2��Һ?
�ο��𰸣���1��2KHCO3![]() ���������
���������
�����Ѷȣ�һ��
3������� ��ѧ������̫���ֽܷ�ˮ���ɵ������ڴ����������������̼��Ӧ���ɼ״�����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�ء���֪H2(g)��CO(g)��CH3OH(l)��ȼ���ȡ�H�ֱ�Ϊ-285.8 kJ��mol-1��-283.0 kJ��mol-1��-726.5kJ��mol-1����ش��������⣺
(1)��̫���ֽܷ�10molˮ���ĵ�������_____________kJ��
(2)�״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽΪ______________________________��
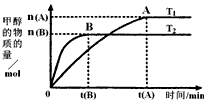
(3)���ݻ�Ϊ2L���ܱ������У���CO2��H2�ϳɼ״����������������������£������¶ȶԷ�Ӧ��Ӱ�죬ʵ������ͼ��ʾ��ע��T1��T2������300�棩������˵����ȷ����________������ţ�
���¶�ΪT1ʱ���ӷ�Ӧ��ʼ��ƽ�⣬���ɼ״���ƽ������Ϊv(CH3OH)=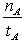 mol��L-1��min-1
mol��L-1��min-1
�ڸ÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ��С
�۸÷�ӦΪ���ȷ�Ӧ
�ܴ���A��ķ�Ӧ��ϵ��T1�䵽T2���ﵽƽ��ʱ����
(4)��T1�¶�ʱ����1molCO2��3molH2����һ�ܱպ������У���ַ�Ӧ�ﵽƽ�����CO2ת����Ϊa���������ڵ�ѹǿ����ʼѹǿ֮��Ϊ__________��
�ο��𰸣�(1)2858
(2)CH3OH(l)+O2(g)
���������
�����Ѷȣ�һ��
4��ѡ���� ���ڷ�ӦX��g��+Y��g���T2Z��g����H��0�������й�˵��������ǣ�������
A����Ӧ�ﵽƽ����������Z�IJ��ʲ��䣬��Ӧ��������
B����Ӧ�ﵽƽ����������¶ȣ�Y��ת��������
C������Ӧ�ڹ̶����ܱ������н��У���ѹǿ���ٱ仯ʱ����Ӧ�ﵽƽ��״̬
D����Ӧ�ﵽƽ�������c��X����ƽ�����ƣ�Kֵ����
�ο��𰸣�A�������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬Z�IJ��ʲ��䣬��Ӧ����
���������
�����Ѷȣ�һ��
5��ѡ���� ����mA��g��+nB��g��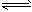 pC��g��+gD��g����ƽ����ϵ���������¶�ʱ����ϵ��ƽ����Է���������
pC��g��+gD��g����ƽ����ϵ���������¶�ʱ����ϵ��ƽ����Է���������
16.9��Ϊ16.5���������ж���ȷ���� [???? ]
A. m+n��p+g ����Ӧ�Ƿ��ȷ�Ӧ
B. m+n��p+g ����Ӧ�����ȷ�Ӧ
C. m+n��p+g �淴Ӧ�Ƿ��ȷ�Ӧ
D. m+n��p+g �淴Ӧ�����ȷ�Ӧ
�ο��𰸣�AC
���������
�����Ѷȣ�һ��