微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
(1)传统哈伯法合成氨工艺中相关的反应式为:N2+3H2
催化剂
△
2NH3 △H<0.
①该反应的平衡常数K的表达式为:K=______.升高温度,K值______(填“增大”“减小”或“不变”).
②不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2的起始物质的量之比为1:3).分析表中数据,______(填温度和压强)时H2转化率最高,实际工业生产不选用该条件的主要原因是______.

③下列关于合成氨说法正确是______(填字母)
A.使用催化剂可以提高氮气的转化率
B.寻找常温下的合适催化剂是未来研究的方向
C.由于△H<0、△S>0,故合成氨反应一定能自发进行
D.增大n(N2):n(H2)的比值,有利于提高H2的转化率
(2)最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法.它既有液氢燃料电池的优点,又克服了液氢不易保存的不足.其装置为用铂黑作为电极,加入电解质溶液中,一个电极通入空气,另一电极通入氨气.其电池反应为
4NH3+3O2=2N2+6H2O
你认为电解质溶液应显______?性(填“酸性”、“中性“、“碱性”),写出负极电极反应式______.
参考答案:(1)①根据化学方程式可写出平衡常数为k=
本题解析:
本题难度:一般
2、选择题 一定温度下将1mol?SO3??放入2L的反应器内,当反应:2SO3(g)

2SO2(g)+O2(g)?平衡时,容器内有0.6molSO2,其平衡常数约是( )
A.0.68
B.0.34
C.0.45
D.0.47
参考答案:B
本题解析:
本题难度:一般
3、选择题 FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+?(aq)+SCN-(aq)?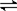 Fe(SCN)2+?(aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T三关系如下图所示,则下列说法正确的是( )
Fe(SCN)2+?(aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T三关系如下图所示,则下列说法正确的是( )
A.FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为:Fe3+(aq)+SCN-(aq)=Fe(SCN)2+(aq)△H>0
B.温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1>K2
C.反应处于D点时,一定有V正>V逆
D.A点与B点相比,A点的c(Fe3+)大
参考答案:BC
本题解析:
本题难度:一般
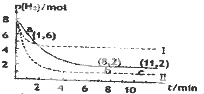
4、选择题 T℃时,将6molCO2和8molH2充入2L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时同的变化,下列说法正确的是( ? )
A.T℃时,该反应的化学平衡常数为0.125
B.反应开始至a点时v(CO2)=1mol?L-1?min-1
C.若曲线I对应的条件改变是升温,则该反应△H<0
D.曲线Ⅱ对应的条件改变是降低压强
参考答案:C
本题解析:
本题难度:简单
5、填空题 “低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式: ___?C+?___?KMnO4+?____?H2SO4→____CO2↑+?____MnSO4?+?____K2SO4+?____H2O??
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中。进行反应
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据
CO2(g)+H2(g),得到如下三组数据
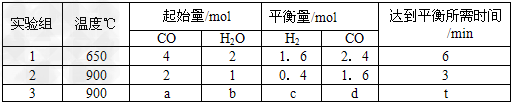
①实验1条件下平衡常数K=________(取小数二位,下同)。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b?的值_______(填具体值或取值范围)。
③实验4,若900℃时,在此容器中加入10molCO,5molH2O,2molCO2,5molH2,则此时
V正_____V逆(填“>”、“<”“=”)。
(3)已知在常温常压下:
①?2CH3OH(l)?+?3O2(g)?=?2CO2(g)?+?4H2O(g)???ΔH?=?-1275.6?kJ/mol
②?2CO?(g)+?O2(g)?=?2CO2(g)???ΔH?=?-566.0?kJ/mol
③?H2O(g)?=?H2O(l)???ΔH?=?-44.0?kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______________________
(4)为最近有科学家提出构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。该构想技术流程如下
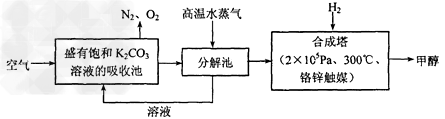
向分解池中通入高温水蒸气的作用是_______________________________
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。
CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mo1/L?,则生成沉淀所需CaCl2溶液的最小浓度为
__________。
参考答案:(1)_5_ C+ _4_ KM
本题解析:
本题难度:一般
网站客服QQ: 960335752 - 14613519 - 791315772