微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 国务院强调“南水北调”工程必须坚持“三先三后”的原则.在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患.检测某工厂废液中,含有大量的Mg2+、Al3+、
Cu2+、Ag+.试分析回答下列问题:
(1)该废液中可能大量存在的一种阴离子是________(选填序号).
A.SO42-???B.NO3-???C.Cl-????D.CO32-
(2)检验废液中铝元素的含量,需将其从废水样品中分离出来,所用的试剂可以是________,铝元素发生变化的离子方程式是______________________.
(3)为了回收废液中的金属银,某同学设计了如下方案
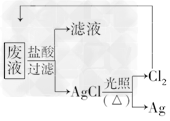
若依该方案获得银108?g,为保证不污染环境和氯气的循环利用,理论上应提供标准状况下的氢气________L.
参考答案:(1)B
(2)NaOH溶液;Al3++4OH-==
本题解析:
本题难度:一般
2、选择题 0.5mol硝酸铵在一定条件下可分解成0.2mol硝酸和16.2g水以及另外一种气态物质,该气态物质可能是
A.NO
B.N2O
C.N2O3
D.N2
参考答案:D
本题解析:分析:16.2g水的物质的量为0.9mol,反应前各种原子的量:1mol N,2mol H,1.5mol O;反应后硝酸与水中含有的原子:2mol H,0.2mol N,1.5molO,所以未知气体中含有:N原子0.8mol,不含H原子、O原子.据此判断.
解答:16.2g水的物质的量为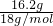 =0.9mol,
=0.9mol,
反应前0.5mol硝酸铵含有的各种原子的物质的量:
N原子0.5mol×2=1mol,H原子0.5mol×4=2mol,O原子0.5mol×3=1.5mol;
反应后硝酸与水中含有的原子:
N原子0.2mol,H原子0.2mol+0.9mol×2=2mol,O原子0.2mol×3+0.9mol=1.5mol.
所以未知气体中含有:N原子1mol-0.2mol=0.8mol,不含H原子、O原子.
所以未知气体为N2.
故选:D.
点评:考查原子守恒的计算,难度不大,关键根据原子守恒判断未知气体中元素种类及原子个数比.
本题难度:简单
3、选择题 下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是 [???? ]
A.NaHSO4和Ba(OH)2
B.AlCl3和NaOH
C.NaAlO2和H2SO4
D.Ba(HCO3)2和Ba(OH)2
参考答案:AD
本题解析:
本题难度:简单
4、选择题 有下列四组物质,如果把某组物质中的后者逐滴加入到前者中至过量,将出现“先产生白色沉淀,后白色沉淀溶解”的现象,这组物质是 [???? ]
A.稀硫酸、氯化钡溶液
B.硫酸亚铁溶液、氢氧化钠溶液
C.氯化钠溶液、硝酸银溶液
D.氯化铝溶液、氢氧化钠溶液
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列各组物质的稀溶液相互反应,把前者逐滴滴入后者与把后者逐滴滴入前者,所产生的现象不相同的是[???? ]
A.AlCl3和NaOH
B.NaCO3和BaCl2
C.NaHCO3和HCl
D.NaCl和AgNO3
参考答案:A
本题解析:
本题难度:简单