微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述中,正确的是
A.在船舶的外壳装上铜块可防止其发生电化学腐蚀
B.MnO2、FeCl3和CuSO4都可加快H2O2的分解速率
C.FeCl3溶 液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
D.用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg
参考答案:B
本题解析:A:在船舶的外壳装上铜块是加快了船体的腐蚀,因为船体是铁,与铜形成原电池时铁做负极,腐蚀更快,为防止其发生电化学腐蚀可加一块比铁活泼的金属,如锌,船体做正极,就被保护了。C:FeCl3溶液溶液加热蒸干、灼烧得到Fe2O3,因为FeCl3水解得到HCl,挥发了,促进水解的进行。Fe2(SO4)3溶液加热蒸干时,水解产物是硫酸,无挥发性,最后产物还是Fe2(SO4)3。
D:用惰性电极分别电解CuCl2溶液时,得到单质Cu,电解MgCl2溶液时,得不到单质Mg,因为氧化性H+>Mg2+,H+先放电
本题难度:一般
2、计算题 400 mL NaNO3和AgNO3的混合溶液中c(NO3―)=4mol/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到11.2L气体(标准状况),假设电解后溶液体积仍为400 mL。试计算
(1)上述电解过程中转移电子的物质的量;
(2)电解后溶液中的C(H+)
参考答案:
本题解析:略
本题难度:简单
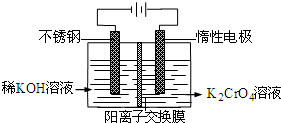
3、选择题 以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如图:下列说法不正确的是( )
A.在阴极式,发生的电极反应为:2H2O+2e-=2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动
C.该制备过程总反应的化学方程式为:4K2CrO4+4H2O
?通电?
.
?
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为1-d
2
参考答案:A、电极均为惰性电极,在阴极室发生还原反应,水得电子变成氢气
本题解析:
本题难度:一般
4、选择题 用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是 [???? ]
A.NaCl溶液?????
B.HCl溶液????
C.NaOH溶液?????
D.AgNO3溶液
参考答案:C
本题解析:
本题难度:一般
5、选择题 在如图装置中,通电一段时间后,乙装置左侧电极质量增加,下列说法不正确
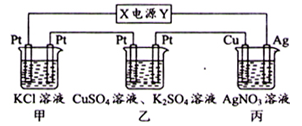
A.向甲中通入适量的HCl气体,可使溶液恢复到电解前状态
B.电解过程中丙中溶液的pH无变化
C.乙中左侧电极质量增加是因为有铜在此电极析出
D.当甲装置中共产生标准状况下0.448 L气体时,丙中Cu电极上质量增加4.32 g
参考答案:D
本题解析:
试题分析:由题给条件乙装置左侧电极质量增加可知为阴极,析出金属铜,从而确定电源X极为负极;且甲中产生H2和 Cl2,通入HCl气体,可使溶液恢复电解前状态;丙中电镀池溶液的pH不变;当甲中产生0.448L气体时,可知转移的电子为0.02mol,所以丙中质量增加为2.16g。
考点:电解原理及计算。
本题难度:困难
|
|
网站客服QQ: 960335752 - 14613519 - 791315772