��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ȡ100 mLNa2CO3��Na2SO4�����Һ����������Ba(OH)2��Һ100 mL��ǡ����ȫ��Ӧ�����ˡ������õ�14.51g��ɫ��������Һ���ټӹ���ϡ���ᴦ�������������ٵ�4.66g����������ų���
(1)д�������������йط�Ӧ�����ӷ���ʽ��_______________________________________
_________________________________________________________________________(4��)
(2)ԭ���Һ��Na2SO4�����ʵ���Ũ��Ϊ_________________ (2��)
�ο��𰸣���1��Ba2+ + CO32- = BaCO3����1�֣� ?
�����������
�����Ѷȣ���
2��ѡ���� ���и����������������Һ�еķ�Ӧ������ͬһ���ӷ���ʽ��ʾ���ǣ�???��
A�������������������������̼��
B��BaCl2��Һ��Na2SO4��Һ��Ba(OH)2��Һ��H2SO4��Һ
C��NaHCO3��Һ��KHSO4��Һ��Ca(HCO3)2��Һ�����HCl��Һ
D����������ϡ�����ϣ�����ͭ��ϡ����
�ο��𰸣�C
���������A�����������������ᷴӦ���ӷ���ʽΪ�����������������ӷ�Ӧ����ˮ��������������̼�ᷴӦ��̼��������ɲ�������ӣ�B����BaCl2��Һ��Na2SO4��Һֻ�������ᱵ��Һ����Ba(OH)2��Һ��H2SO4��Һ��Ӧ���������ᱵ���ˮ���ɣ�C��ȷ��D������������ϡ������Ϊ�������������ӷ�Ӧ��������ͭ��ϡ���ᷴӦ������ͭ�������ӷ�Ӧ��
�����Ѷȣ�һ��
3��ѡ���� �������ӷ���ʽ��ȷ����
A�������ȥˮ���е�CaCO3��CaCO3��2H+=Ca2+��H2O��CO2��
B����ˮ��ͨ��������SO2��I2 +SO2+2H2O=2I��+SO42��+4H+
C��NaHSO4��Һ��Ba(OH)2��Һ��Ӧ�����ԣ�H+��SO42����Ba2+��OH��=BaSO4����H2O
D����ǿ����Һ�д���������Fe(OH)3��Ӧ����Na2FeO4��
3ClO��+2Fe(OH)3=2FeO42��+3Cl��+H2O+4H+
�ο��𰸣�B
���������
���������A������ȷ��CaCO3��2CH3COOH=Ca2����2CH3COO�D��H2O��CO2��;B����ȷ��C������ȷ��2H+��SO42����Ba2+��2OH��=BaSO4����2H2O��D������ȷ��������ǿ�����ʽ��ȴд����������������ѡB��
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ��ȷ���ǣ�������
A������������Һ��������Һ��ϣ�Ba2++SO42-�TBaSO4��
B������ϡ���ᷴӦ��Fe+2H+�TFe2++H2��
C����ͭƬ�����Ȼ�����Һ�У�Fe3++Cu�TFe2++Cu2+
D���Ȼ�����Һ�м��������ˮ��Al3++3NH3?H2O�TAl��OH��3��+3NH4+
�ο��𰸣�A������������Һ��������Һ��Ӧ����BaSO4��H2O����Ӧ��
���������
�����Ѷȣ���
5��ѡ���� ���н�����ʵ�ķ���ʽ����ȷ���ǣ�???��
A����0.1mol/L��ˮ��pHΪ11��NH3��H2O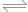 NH4++OH-
NH4++OH-
B����Na�����ˮ�У��������壺2Na+2H2O=2NaOH+H2��
C����CuCl2��Һ������ʵ�飬���ݷ��⣺CuCl2 Cu2++2Cl-
Cu2++2Cl-
D��AlƬ����NaOH��Һ�У��������壺2Al+2OH-+2H2O=2AlO2-+3H2��
�ο��𰸣�C
���������
���������A����ˮΪ������ʣ����ڵ���ƽ�⣬��ȷ��B��Na���ʷdz����ã�����ˮ��Ӧ�ų�H2����ȷ��C�����뱾������Ҫͨ�磬�ʷ���ʽ����D��Al����NaOH��Һ��Ӧ�ų���������ȷ��
�����Ѷȣ�һ��