?
现象:???????????????????????????;
结论:????????????????????????????。
?
(4)用碘量法测量自来水中残留的Cl2的浓度:
① 在大锥形瓶中放置过量的KI,加一定量的冰醋酸,准确取水样200mL加入瓶中,迅速塞上瓶塞摇动,水样呈淡黄色,发生反应:Cl2+2I-=2Cl-+ I2。
②加少许淀粉溶液,用cmol/L Na2S2O3溶液滴定,发生反应:I2+2S2O32-=2I-+S4O62-,当????????????????????????????????????????????????????????????,达到滴定终点。
③重复操作3次,平均读数为V mL,则该样品中残留Cl2的浓度:?????????mg/L(Cl的相对原子质量:35.5)
参考答案:(16分)
(1) NaCl + NH3 + CO2
本题解析:
试题分析:(1)氨气易溶于饱和食盐水,且NH3+H2O=NH3?H2O,得到氯化钠、氨水溶液;一水合氨是弱碱,二氧化碳是酸性氧化物,不断通入二氧化碳气体时,NH3?H2O+CO2=NH4HCO3;由于碳酸氢钠的溶解度比氯化钠、碳酸氢铵都小,碳酸氢钠最先达到饱和,则碳酸氢铵与氯化钠容易反应,生成碳酸氢钠晶体和氯化铵溶液,即NH4HCO3+NaCl=NaHCO3↓+NH4Cl;上述几步反应加起来可得:NaCl + NH3 + CO2 + H2O = NaHCO3 ↓+ NH4Cl;(2)碳酸氢钠是固体
本题难度:困难
2、填空题 (14分) 某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装 某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及下图所示装
置制取NaHCO3,反应的化学方程式为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl。然后再将NaHCO3制成
Na2CO3。
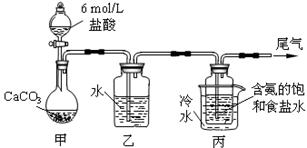 
(1)装置乙的作用是??????????????????????????????????????????。为防止污染空气,尾气中含有的??????????需要进行吸收处理。
(2)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有????????、 ????????、???????。
NaHCO3转化为Na2CO3的化学方程式为?????????????????。
(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热了t1 min的NaHCO3 样品的组成进行了以下探究。
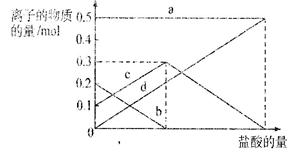
取加热了t1 min的NaHCO3样品29.6 g完全溶于水制成溶液,然后向此溶液中缓慢地滴加稀盐酸,并不断搅拌。随着盐酸的加入,溶液中有关离子的物质的量的变化如右图所示。
则曲线c对应的溶液中的离子是???????????????
(填离子符号);该样品中NaHCO3和Na2CO3的物质的量之比是???????????。
(4)若取21. 0 g NaHCO3固体,加热了t2?min后,剩余固体的质量为l4.8 g。如果把此剩余固体全部加入到200 mL 2 mol・L-1的盐酸中则充分反应后溶液中H+ 的物质的量浓度为____________(设溶液体积变化忽略不计)。
参考答案:(1)除去二氧化碳中的氯化氢气体(2分)??????????
本题解析:
试题分析:(1)装置甲是制备二氧化碳气体的反应装置,生成的二氧化碳气体中含有氯化氢气体,对制备碳酸氢钠有影响,装置乙的作用是吸收氯化氢气体;最后的尾气中含有氨气不能排放到空气中,需要进行尾气吸收;故答案为:吸收HCl;NH3;(2)由装置丙中产生的NaHCO3发生的反应为,NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl;制取Na2CO3时需要过滤得到晶体,洗涤后加热灼烧得到碳酸钠;故答案为:过滤、洗涤、灼烧;(3)若在(2)中灼烧的时间较短,NaHCO3将分解不完全,该小组对一份加热
本题难度:困难
3、选择题 有关Na2CO3和NaHCO3的叙述中正确的是
A.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1:2
B.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
C.物质的量浓度相同时,Na2CO3溶液的pH小于NaHCO3溶液
D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出
参考答案:D
本题解析:略
本题难度:一般
4、选择题 下列金属单质中,不能从CuCl2溶液中置换出铜的是(???)
A.锌
B.镁
C.钠
D.铁
参考答案:C
本题解析:
试题分析:钠的金属性虽然强于铜的,但钠太活泼,投入水中立即生成氢氧化钠和氢气,不能置换出铜,其余选项都是可以的,答案选C。
点评:该题是基础性试题的考查,难度不大,该题的关键是明确常见金属的化学性质,然后灵活运用即可,学生不难得分。
本题难度:简单
5、选择题 ①钾的密度比水小;②钾的熔点较低;③钾与水反应时要放出热量;④钾与水反应后溶液呈碱性。某学生将一小块金属钾投入滴有酚酞试液的水中,此实验能证明上述四点性质中的(???)
A.①④
B.①②④
C.①③④
D.①②③④
参考答案:D
本题解析:K元素的原子结构与Na很相似,因此K的性质可完全类比于Na的性质,只是比Na与水的反应更剧烈。
本题难度:简单
|