微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述中正确的是
A.H2SO4的摩尔质量是98
B.CO的摩尔质量为28 g/ mol
C.1 molO的质量是16g/ mol
D.将98gH2SO4溶解于500 mL水中,所得溶液中H2SO4的物质的量浓度为2 mol/L
参考答案:B
本题解析:A错,H2SO4的摩尔质量是98 g/ mol;B正确;C错,1 molO的质量是16g;D错,不知道溶液的体积无法计算;
本题难度:一般
2、计算题 取1.43 g Na2CO3・xH2O溶于水配成10 mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸2.0 mL,并收集到112 mL CO2(标准状况)。试计算:
(1)CO2的物质的量。
(2)Na2CO3・xH2O的物质的量。
(3)x的值。
(4)所用稀盐酸的物质的浓度。
参考答案:
(1)0.005mol
(2)0.005mol
本题解析:
试题分析:
n(CO2)=0.112L/22.4L/mol=0.005mol,
Na2CO3+2HCl=2NaCl+CO2↑+H2O
1????? 2??????????????? 1
n(Na2CO3)??n(HCl)????0.005mol
(1)n(CO2)=0.112L/22.4L/mol=0.005mol;
(2)n(Na2CO3?xH2O)=n(Na2CO3)=0.005mol,
M(Na2CO3?xH2O)=286g/mol,故答案为:2
本题难度:一般
3、计算题 (6分)计算题(写出计算过程)
将11g铝铁合金的粉末放入100mL过量的KOH溶液中充分反应,得到标准状况下6.72L H2。试计算:
(1)该合金中铝的质量分数(保留两位有效数字);
(2)该合金中铝和铁的物质的量之比。
参考答案:(1)49%(2)2:1
本题解析:
试题分析:(1)2Al+2KOH+2H2O=2KAlO2+3H2 ↑,所以生成6.72升氢气,即6.72/22.4=0.3摩尔氢气,反应的铝的物质的量为0.2摩尔,质量为0.2×27=5.4克,所以铝的质量分数=5.4/11=49%。(2)铁的质量为11-5.4=5.6克,物质的量为5.6/56=0.1摩尔,所以铝和铁的物质的量比为0.2:0.1=2:1。
考点:铝的性质。
本题难度:一般
4、选择题 设NA为阿伏加德罗常数,如果ag某气态双原子分子的分子数为P,则bg该气体在标准状况下的体积V(L)是
A.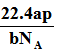
B.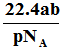
C.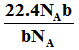
D.
参考答案:D
本题解析:
试题分析:ag某气态双原子分子的分子数为P,则bg该气体的分子个数是N=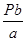 ,其物质的量是
,其物质的量是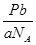 ,所以在标准状况下的体积是V=n?Vm=
,所以在标准状况下的体积是V=n?Vm=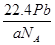 ,故选项是D。
,故选项是D。
考点:考查物质的量与物质的分子数、气体的体积和阿伏伽德罗常数的关系的知识。
本题难度:一般
5、选择题 下列物质中,在标准状况下体积最大的是(?)
A.900g H2O
B.71g Cl2
C.48g O2
D.28g N2
参考答案:C
本题解析:
试题分析:A、水在标准状况下为液体,900gH2O的体积为0.9L;B、Cl2的物质的量为 ?=1mol,22.4L;C、O2的物质的量为
?=1mol,22.4L;C、O2的物质的量为 本题难度:一般
本题难度:一般