微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键 [???? ]
A.一定是离子键????
B.一定是共价键 ??
C.可能是离子键,也可能是共价键????
D.以上说法都不正确
参考答案:C
本题解析:
本题难度:简单
2、填空题 太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺人Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。
(1)镓的基态原子的电子排布式是___??????。
(2)硒为第4周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为???(用元素符号表示)。
(3)H2Se的酸性比H2S____(填“强”或“弱”)。气态SeO3分子的立体构型为____????。
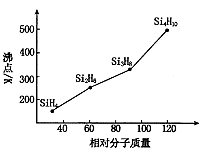
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是?????。
(5)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]―而体现一元弱酸的性质,则[B(OH)4]―中B的原子杂化类型为??????????????????。
(6)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是____,反应的离子方程式为????????????。
(7)一种铜金合金晶体具有面心立方最密堆积的结构。在晶脆中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为?????,若该晶胞的边长为a pm,则合金的密度为????g・cm-3(已知lpm=10-12m,只要求列算式,不必计算出数值,阿伏加塞罗常数为NA)。
参考答案:(15分)
⑴1s22s22p63s23p63d104
本题解析:
试题分析:⑴31号元素镓的基态原子的电子排布式是1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1)
⑵一个周期从左往右第一电离能呈增大趋势,故硒、砷和溴元素的第一电离能从大到小顺序为Br>As>Se
⑶第ⅥA氢化物水溶液酸性由弱变强,故H2Se的酸性比H2S强。气态SeO3分子的立体构型为平面三角形。
⑷[B(OH)4]―中B的原子结合4个羟基,杂化类型为sp3。
⑸组成和结构相似的分子,相对分子质量越大,分子间范德华力越强,沸点越高。
本题难度:困难
3、选择题 某品牌食品包装中放有一包用作干燥剂的生石灰,生石灰的主要成分是( )
A.CaCO3
B.Ca(OH)2
C.CaSO4
D.CaO
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列有关化学用语的表示正确的是
[???? ]
A.过氧化氢的电子式为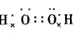
B.聚氯乙烯的结构简式为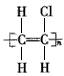
C.Na+的结构示意图为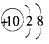
D.乙烯的结构式为 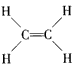
参考答案:D
本题解析:
本题难度:简单
5、填空题 Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其同态属于_____________晶体,俗名叫_______________;
(2)R的氢化物分子的空间构型是___________,属于__________分子(填“极性”或“非 极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是_________________
(3)X的常见氢化物的空间构型是______________;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是____________________
(4)Q分别与Y、Z形成的共价化合物的化学式是___________和___________;Q与Y形成的分子的电子式是_______________,属于___________分子(填“极性”或“非极性”)。
参考答案:(1)分子;干冰
(2)正四面体;非极性;Si3N4<
本题解析:
本题难度:一般