微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图所示,将铁棒和石墨棒插入1 L 1 mol・L-1食盐水中。下列说法正确的是( )
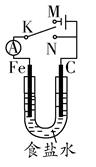
A.若电键K与N连接,铁被保护不会腐蚀
B.若电键K与N连接,正极反应式是4OH--4e-=2H2O+O2↑
C.若电键K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜
D.若电键K与M连接,当两极共产生28 L(标准状况)气体时,生成了1 mol NaOH
参考答案:D
本题解析:A项,若电键K与N连接,则形成原电池,铁作负极,被腐蚀,不正确;B项,若电键K与N连接,正极反应式是O2+2H2O+4e-=4OH-,不正确;C项,若电键K与M连接,将石墨棒换成铜棒,则形成电解池,若要在铁棒上镀铜,电解质溶液不能用食盐水,而应用硫酸铜溶液,故不正确;D项,若电键K与M连接,为电解食盐水,根据反应方程式:
2NaCl+2H2O 本题难度:一般
本题难度:一般
2、填空题 (12分)某实验小组的同学对电化学原理进行了一系列探究活动
(1)如图为某实验小组依据氧化还原反应:(用离子方程式表示) 设计的原电池装置,反应前,两电极质量相等,一段时间后,两电极质量相差18g,则导线中通过 mol电子。
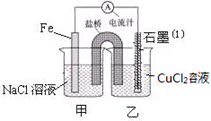
(2)用胶头滴管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,写出发生反应的离子方程式 ,然后滴加几滴硫氰化钾溶液,溶液变红;继续滴加过量新制饱和氯水,红色褪去,假设之一是“溶液中的+3价铁被氧化为更高的价态”。如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。
(3)如图其它条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,石墨(1)为 极(填“正”、“负”、“阴”或 “阳”)。在甲装置中滴加几滴酚酞试液,振荡均匀,一段时间后,在甲装置中观察到 电极(填“铁”或“铜”)附近溶液先变红,该电极的反应式为 。

参考答案:(12分)
(1)Fe+Cu2+==Fe2++Cu (
本题解析:
试题分析:(1)根据该原电池的电解质溶液及电极,判断该原电池的反应原理是Fe与铜离子的置换反应,离子方程式是Fe+Cu2+==Fe2++Cu;在该电池中Fe作负极,失去2个电子生成亚铁离子进入溶液,而石墨极为正极,铜离子得到2个电子生成Cu单质析出,开始两电极的质量相等,负极质量减少56g,则正极质量增加64g,两极的质量差为56g+64g=120g,所以当两电极质量相差18g时,有18/120mol=0.15molFe失去电子,则转移电子的物质的量是0.3mol;
(2)铁片附近的溶液中含有亚铁离子,滴加氯水,则氯气与亚铁离子反应生成铁离子和氯离子,离子方程式是2Fe2++Cl2==2Fe3++2Cl-;铁离子与KSCN溶液反应,溶液变红色;继续滴加过量新制饱和氯水,红色褪去,假设之一是“溶液中的+3价铁被氧化为更高的价态”。如果+3价铁被氧化为FeO42-,则氯气被还原为氯离子,根据元素守恒,则该反应中有O元素参与,所以反应中还有谁参加,生成物中有氢离子生来源:91考试网 91exam.org成,离子方程式是2Fe3++3Cl2+8H2O==2FeO42-+6Cl-+16H+;
(3)若将盐桥换成弯铜导线与石墨相连成n型,则该装置为原电池和电解池的串联装置,甲池为原电池,乙池为电解池,Fe作负极,Cu为正极,则石墨极为电解池的阴极;甲为Fe的吸氧腐蚀反应,正极为氧气得到电子,与水结合生成氢氧根离子,Cu极附近溶液呈碱性,所以Cu极附近先变红色;该电极的反应式是O2+4e-+2H2O==4OH-。
考点:考查电化学反应原理的应用
本题难度:一般
3、选择题 汽车的启动电源常用铅蓄电池,放电时其电池反应如下:PbO2+Pb+2H2SO4="=" 2PbSO4+2H2O。根据此反应判断,下列叙述中正确的是
A.Pb是正极
B.PbO2得电子,被氧化
C.负极反应是Pb+SO42――2e―="=" PbSO4
D.电池放电时,溶液酸性增强
参考答案:C
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。根据反应式可知,铅失去电子,二氧化铅得到电子,所以铅是负极,二氧化铅是正极。选项C是错误的,答案选C。
本题难度:一般
4、选择题 某原电池总反应离子方程式为Mg+2H+=Mg2++H2↑能实现该反应的原电池是( )
A.正极为铜,负极为镁,电解质溶液为稀盐酸
B.正极为铜,负极为铁,电解质溶液为稀硫酸
C.正极为石墨,负极为镁,电解质溶液为CuSO4溶液
D.正极为银,负极为镁,电解质溶液为NaCl溶液
参考答案:电池反应式Mg+2H+=Mg2++H2↑知镁发生氧化反应作负
本题解析:
本题难度:简单
5、选择题 有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为:C2++2e-→C,B―2e-→B2+则A、B、C、D金属性由强到弱的顺序为( )
A.A>B>C>D B.A>B>D>C C.D>A>B>C D.D>C>A>B
参考答案:C
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。据此可判断,选项C是正确的,答案选C。
本题难度:一般