微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在标准状况下,mg气体A与ng气体B的分子数相同,下列说法不正确的是( )。
A.气体A与B的相对分子质量之比是m∶n
B.相同质量的气体A与B的分子数之比是n∶m
C.同温同压下气体A与B的密度之比为n∶m
D.相同状况下,同体积气体A与B的质量比为m∶n
参考答案:C
本题解析:mg气体A与ng气体B的分子数相同,则A与B的摩尔质量之比是n∶m,选项A不正确;相同质量的气体A与B的分子数之比是m∶n,选项B不正确;同温同压下气体的密度之比是相应的摩尔质量之比,所以选项C正确;相同状况下,同体积气体A与B的质量比为n∶m,选项D不正确,因此正确的答案选C。
本题难度:一般
2、选择题 在aLAl2(SO4)3和(NH4)2SO4的混合溶液中加入bmolBaCl2,恰好使溶液中的SO42-离子完全沉淀;如加入足量强碱并加热可得到cmol NH3,则原溶液中的Al3+浓度(mol/L)为
[???? ]
A.
B.
C.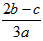
D.
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列关于 0.2 mol/L 硝酸钾溶液的叙述中,正确的是 ( )
A.1 L该溶液中含硝酸钾 202 g
B.100 mL 该溶液中含硝酸钾 0.02 mol
C.从 1 L 该溶液中取出 500 mL 后,剩余溶液的浓度为 0.1 mol/L
D.1 L水中溶解 0.2 mol 硝酸钾,即可配得 0.2 mol/L 硝酸钾溶液
参考答案:B
本题解析:
试题分析:A.n="c・V=0.2" mol/L×1L=0.2mol,m="n・M=0.2mol×101g/mol=20.2" g,错误;B.n="c・V=0.2" mol/L×0.1L=0.02mol,正确;C.溶液有均一性,无论取出多少,溶液的浓度相等,因此剩余溶液的浓度为 0.2 mol/L,错误;D.应该是溶液的体积而不能是溶剂的体积,故该选项错误。
考点:考查有关溶液的物质的量浓度的说法的知识。
本题难度:一般
4、选择题 设 NA为阿伏加德罗常数的数值,下列说法正确的是
A.NA个CH4分子的质量为16g/mol
B.1mol/LNaCl溶液含有NA个Na+
C.等物质的量的N2和CO所含分子数相同
D.22.4LCO2中含有 NA个CO2分子
参考答案:C
本题解析:
试题分析:质量的单位是g。所以A错;B中只给出了浓度,没有体积,所以不能算出钠离子的个数。B错;由n="N/" NA得,等物质的量的N2和CO所含分子数相同,正确。D中,给出体积没有指名温度和压强,所以个数无法确定,D错,故选C。
考点:NA的应用
点评:熟悉和物质的量有关的物理量,物质的量浓度,气体摩尔体积,质量,阿伏伽德罗常数等,此类问题便不难解决。
解答阿伏加德罗常数(NA)问题的试题时,必须注意下列一些细微的知识点:
①标准状况下非气体物质:水、溴、SO3、CCl4、苯、辛烷、CHCl3等不能用Vm=22.4L/mol将体积转化为物质的量。
②分子中原子个数问题:氧气、氮气、氟气等是双原子的分子,稀有气体(单原子分子)、白磷(P4)、臭氧(O3)。
③较复杂的氧化还原反应中转移的电子数:Na2O2与H2O、Cl2与NaOH、KClO3与盐酸、铜与硫、电解AgNO3等。
本题难度:困难
5、选择题 旨在限制发达国家温室气体排放量,抵制全球内气候持续变暖的《京都议定书》于2005年2月16日正式生效.我国二氧化碳排放量居世界第二,下列减少二氧化碳的措施不切实际的是
A.积极开发新能源
B.充分利用新能源
C.不使用化学能源
D.积极开发核能源
参考答案:C
本题解析:分析:减少二氧化碳的排放,可积极开发、使用清洁能源,减少化石能源的使用.
解答:积极开发新能源、充分利用新能源、积极开发核能源都可减少化石能源的使用,可减少二氧化碳的排放,但大多数能源都属于化学能源,不使用化学能源不实际.
故选C.
点评:本题考查化学污染及治理,题目难度不大,注重相关基础知识的积累,本题注意氢能、电能等都与化学能源有关.
本题难度:困难