��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����1 mol HCl��1 mol MgSO4�Ļ����Һ�м���1 mol/L Ba(OH)2��Һ������ͼ������ȷ��ʾ�������������ʵ���(n)�����Ba(OH)2��Һ�����(V)֮���ϵ����(����)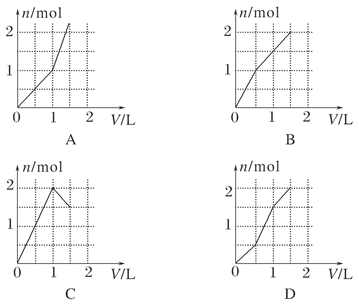
�ο��𰸣�D
�������������Ba(OH)2���ᷢ��H����OH��===H2O��Ba2����SO42��===BaSO4����Mg2����2OH��===Mg(OH)2����������0.5 mol Ba(OH)2ʱ����������ٵ��������BaSO4����������Mg(OH)2������������Ba(OH)2 1 molʱSO42��������ȫ������1.5 mol Ba(OH)2ʱ��Mg2���ֳ�����ȫ����ѡD��
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��ȷ����
A.NaHCO3��Һ��NaAlO2��Һ��ϣ�HCO3-+AlO2-+H2O=Al��OH��3��+CO32-
B.Al��OH��3���룺H2O+AlO2-+H+�TAl��OH��3�TAl3++3OH-
C.HF����ˮ��HF+H2O�TH3O++F-
D.Na2S����ˮ��S2-+2H2O�TH2S+2OH-
�ο��𰸣�A
���������������A����Ӧ��������������̼���ƣ�
B��Al��OH��3Ϊ�����������������ʽ�ͼ�ʽ���룻
C��HF���
D��������ˮ��ֲ����У��Ե�һ��Ϊ����
���A��NaHCO3��Һ��NaAlO2��Һ��ϵ����ӷ�ӦΪHCO3-+AlO2-+H2O=Al��OH��3��+CO32-����A��ȷ��
B��Al��OH��3����Ϊ��H2O+AlO2-+H+?Al��OH��3?Al3++3OH-��Ϊ���淴Ӧ����B����
C��HF����ˮ���ڵ���ƽ��ΪHF+H2O?H3O++F-����C����
D��Na2S����ˮ��ˮ�����ӷ�ӦΪS2-+H2O?HS-+OH-����D����
��ѡA��
���������⿼�����ӷ�Ӧ����ʽ����д���漰�ٽ����롢����ƽ�⡢ˮ��ƽ������ӷ�Ӧ��ע����淴Ӧ�á�?������Ŀ�ѶȲ���
�����Ѷȣ�һ��
3������� ij��Һ�д���Na����AlO2����CO32����OH���������Һ�еμ����ᣬ�ʲ��������˳����ʲô��д����ص����ӷ���ʽ��
�ο��𰸣���һ��ʱ�䱣��ԭ�� H����OH��=H2O���ڿ�ʼ������������
���������
������������ڷ�������ԭ��Ӧ(Ҳ���Ǹ��ֽⷴӦ)�����ӷ�Ӧ��,������ͨ�������������Ի�ԭ�ԱȽϵķ���������,������ԱȽϸ���,���ǿ����ü��跨�������
�����⡿��ΪAlO2����CO32����OH����Ҫ��H+��Ӧ����Ӧ���£�
H����AlO2����H2O=Al(OH)3��????Al(OH)3��3H��=Al3����3H2O ???????��
CO32����H��=HCO3��????????????? HCO3����H��=CO2����H2O??????????��
H����OH��=H2O???
�����Ѷȣ�һ��
4��ѡ���� ij��Һ�к���HCO3-��SO32-��Cl-��Na+����������ͨ��������Cl2����Һ�������������ӵ�Ũ�Ȼ������ֲ������
[???? ]
A��HCO3-
B��SO32-
C��Cl-
D��Na+
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ij�����ӻ�������ɵĻ����ֻ���ܺ������������е������֣�K����NH4+��Mg2+��Ba2+��Cl����CO32����SO42����Ϊȷ������ɣ�ȷ��ȡ14.82g���������ˮ��300 mL������Һ���ֳ����ȷݷֱ��������ʵ�飺
��1����һ�ݼ���AgNO3��Һ�г�������
��2���ڶ��ݼ�����NaOH��Һ�����ȣ�����ʯ�Ҹ�����ռ������������1.12L
��3�������ݼ�����BaCl2��Һ��������ϴ�ӡ���������Ϊ6.27g����������м��������ᣬ�����ˡ�ϴ�ӡ���������Ϊ2.33 g
��������ʵ�飬�����Ʋⲻ��ȷ����
A����Һ��c(SO42��)Ϊ0.1mol/L��c(CO32��) Ϊ0.2mol/L
B���û�����в���Ba2+��Mg2+
C��һ������NH4+�� K������ȷ��Cl���Ƿ����
D��ʵ�飨3�������м��������ֻ���ˡ���ϴ�ӣ���Գ�NH4+����������Ӻ����IJⶨ���Ӱ��
�ο��𰸣�A
���������
�������������AgNO3��Һ�г���������������Cl-��CO32-��SO42-���ڼ�����NaOH��Һ���Ȳ������壬�����ǰ�������һ���������0.04mol���۲����������2.33gΪ���ᱵ�����ʵ�����0.01mol��6.27g���������ᱵ��̼�ᱵ��̼�ᱵ����Ϊ6.27g-2.33g=3.94g�����ʵ���Ϊ0.02mol����һ������CO32-��SO42-�����һ��û�� Mg2+��Ba2+��c(CO32-)=0.02��0.1=0.02��mol/L�����ٸ��ݵ���غ㣬�����Ϊ��n��+��=n��NH4+��=0
�����Ѷȣ�һ��