微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)(1)写出下列反应的离子方程式:
①氯化铵溶液和氢氧化钠溶液反应 ;
②少量二氧化碳通入澄清石灰水 ;
③三氧化二铁和盐酸反应 。
(2)铜和浓硫酸发生反应的化学方程式为:Cu +2H2SO4(浓)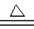 CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
参考答案:19.(10分)(1)①NH4++OH- ===NH3・H2
本题解析:
试题分析:(1)根据离子方程式的书写规则,可写出:①氯化铵溶液和氢氧化钠溶液反应NH4++OH- ===NH3・H2O;②少量二氧化碳通入澄清石灰水CO2+Ca2++2OH- ===CaCO3↓+H2O;③三氧化二铁和盐酸反应Fe2O3+6H+===2Fe3++3H2O。(2)Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O,其中硫元素由+6价降低到+4价,被还原,发生还原反应;浓H2SO4作氧化剂,具有氧化性。
CuSO4+SO2↑+2H2O,其中硫元素由+6价降低到+4价,被还原,发生还原反应;浓H2SO4作氧化剂,具有氧化性。
考点:考查离子方程式的书写,氧化还原反应。
本题难度:一般
2、选择题 下列离子中,只有还原性的是
A.Na+
B.Fe2+
C.Br―
D.SO32―
参考答案:C
本题解析:
试题分析:A. Na+是阳离子,化合价为最高价,所以只有氧化性,错误;B. Fe2+处于该元素的中间价态,既有氧化性,也有还原性,错误;C.Br―处于该元素的最低化合价,只有还原性,正确;D. SO32―其中的S元素处于该元素的中间价态,既有氧化性,也有还原性,错误;
本题难度:简单
3、选择题 根据下列三个反应的化学化学方程式,判断下列关系式不正确的是
(1)I2+SO2+2H2O===H2SO4+2HI??? (2)2FeCl3+2HI===2FeCl2+2HCl+I2
(3)2FeCl2+Cl2===2FeCl3???????????????
?
A.氧化性:Cl2>Fe3+>I2>H2SO4
B.还原性:SO2>I->Fe2+>Cl-
C.2Fe+3I2===2FeI3
D.FeI2+Cl2===FeCl2+I2(Cl2不足时)
参考答案:C
本题解析:
试题分析:C项:氧化性:Fe3+>I2,应生成FeI2,故错。故选C。
点评:本题考查氧化还原反应,明确还原剂、氧化剂中元素的化合价变化是解答本题的关键,并熟悉常见的氧化还原反应来解答。
本题难度:一般
4、填空题 (4分)过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填空:
A.Na2O2 +2HCl= 2NaCl+H2O2
B.Ag2O+ H2O2=2Ag+O2+ H2O
C.2 H2O2="2" H2O+O2
D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O
(1)H2O2仅体现氧化性的反应是(填代号)???????????????。
(2)H2O2既体现氧化性又体现还原性的反应是(填代号)??????????。
(3)上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是:???????????????。
参考答案:
(1)D?(2)C?(3)Ag2O>H2O2&
本题解析:略
本题难度:一般
5、选择题 有一种酸性溶液中存在NO3―、I―、Cl―、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推断溶液中
A.一定含有I―,不能确定是否有Cl―
B.一定含有NO3―
C.可能含有Fe3+
D.一定含有I-、NO3―和Cl―
参考答案:A
本题解析:
试题分析:强酸性溶液中不可能同时存在NO3-、Fe3+与I-,加入溴水后,溴作氧化剂,被还原,说明溶液中不存在比溴氧化性强的物质,所以不存在硝酸根离子;因为溴不与Cl-、Fe3+反应,则溴只能与I-发生氧化还原反应,则溶液中一定存在I-,所以铁离子肯定不存在,氯离子不能确定,则答案选A。
考点:考查离子的检验与判断
本题难度:一般