微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有关物质的量浓度溶液配制 的下列说法中正确的是(????)
的下列说法中正确的是(????)
A.将1mol NaCl溶于1L水中所得溶液物质的量浓度为1mol・L-1
B.将0.1mol NaCl投入100mL容量瓶中加水至刻度线,充分振荡后,浓度为1 mol・L-1
C.需要48mL 0.1 mol・L-1的Na2CO3溶液,配制时应选用50mL容量瓶
D.将4.0g NaOH放入烧杯并加水搅拌冷却后全部转移到1000mL容量瓶中,加水至刻度,所得溶液的浓度为1 mol・L-1
参考答案:C
本题解析:略
本题难度:简单
2、选择题 用下列实验装置进行相应实验,能达到实验目的的是
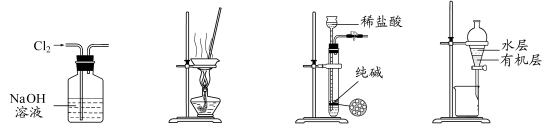
图2?????????????图3??????????????图4????????????????图5
A.用图2 所示装置除去Cl2中含有的少量HCl
B.用图3 所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图4 所示装置制取少量纯净的CO2气体
D.用图5 所示装置分离CCl4萃取碘水后已分层的有机层和水层
参考答案:D
本题解析:A项,NaOH可以将Cl2、HCl同时除去,错;B项,蒸干NH4Cl时,它会分解,错;C项,纯碱为粉未状,不能放于带孔的板上,同时制得的CO2中会混有HCl和H2O,错;D项,CCl4的密度比水大,位于水的下层,正确。
【考点定位】化学实验基本操作
本题难度:一般
3、实验题 重铬酸钠(Na2Cr2O7?2H2O)俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿(主要成份为FeO?Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如下:
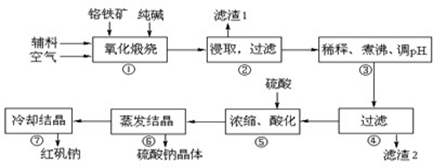
中涉及的主要反应有:
主反应:4FeO?Cr2O3+8Na2CO3+7O2? 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
副反应: SiO2+Na2CO3 Na2SiO3+CO2↑?????? Al2O3+Na2CO3
Na2SiO3+CO2↑?????? Al2O3+Na2CO3 2NaAlO2+CO2↑
2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
沉淀物
| Al(OH)3
| Fe(OH)3
| Mg(OH)2
| Cr(OH)3
|
完全沉淀时溶液pH
| 4.7
| 3.7
| 11.2
| 5.6
?
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是?????????????;
(2)“③”中调节pH至4.7,目的是????????????????????;
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:????????????????????;
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL?2mol?L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol?L-1Na2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)
①判断达到滴定终点的依据是: ?????????????????????。
②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度??????(设整个过程中其它杂质不参与反应) 。
参考答案:(1)使反应物接触更充分,加快反应速率;?
(2)除去
本题解析:
试题分析: (1)反应①反应时不断搅拌目的是加快反应速率。
(2)氧化煅烧后过滤,滤液中阴离子主要含有CrO42-、AlO2-、SiO32-,由表格中信息可知,调节pH至4.7目的是除去溶液中AlO2-、SiO32-。
(3)CrO42-与H+生成Cr2O72-和水。
(4)发生的反应为Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O、I2+2S2O32-=2I-+S4O62-,Cr2O72-~3I2~6S2O32-,所以Na2Cr2O7纯度为= 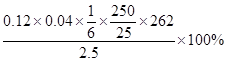 ?=83.84%。淀粉遇碘显蓝色,加入硫代硫酸钠溶液将碘反应完全后溶液呈无色,所以当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色变为无色且30s不变色为终点。 ?=83.84%。淀粉遇碘显蓝色,加入硫代硫酸钠溶液将碘反应完全后溶液呈无色,所以当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色变为无色且30s不变色为终点。
本题难度:困难
4、选择题 下列叙述中正确的是
A.某溶液加入CCl4,C Cl4层显紫色,证明原溶液中存在I-
B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
C.液溴易挥发,在存放液溴的试剂瓶中应加水封
D.硝酸亚铁溶液中要加入稀硝酸抑制水解,防止溶液变浑浊
参考答案:C
本题解析:
试题分析:A、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在单质碘,A不正确;B、能使润湿的淀粉KI试纸变成蓝色的物质不一定是Cl2,凡是能把碘化钾氧化生成单质碘的气体均可,B不正确;C、液溴易挥发,因此在存放液溴的试剂瓶中应加水封防止液溴挥发,C正确;D、在酸性条件下NO3-具有氧化性,能氧化Fe2+,因此硝酸亚铁溶液中加入稀硝酸,发生氧化还原反应生成硝酸铁、NO和水,得不到实验目的,D不正确,答案选C。
本题难度:一般
5、选择题 下列实验操作中,错误的是[???? ]
A.配制5%食盐溶液时,将称量的食盐放入烧杯中加计量的水搅拌溶解
B.硫酸铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2-3次
D.配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
参考答案:D
本题解析:
本题难度:简单
|