微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列特点中,所谓“合金”必须具有的是
(1)具有金属特性?? (2)通过熔合加工?? (3)有两种或两种以上金属(或金属与非金属)? (4)铸造性很好
A.(1)(2)(3)
B.(1)(3)(4)
C.(2)(4)
D.(1)(4)
参考答案:A
本题解析:合金的定义:有两种或两种以上金属(或金属与非金属),通过熔合加工,具有金属特性的物质,所以,“合金”必须具有的是(1)(2)(3),故选A。
本题难度:一般
2、填空题 (14分)利用废铁丝、硫酸铜废液(含硫酸亚铁)和被有机物污染的废铜粉制备硫酸铜晶体。生产过程如下:

试回答下列问题:
(1)铁丝在投入硫酸铜废液前需用稀H2SO4进行处理,可能发生反应的离子方程式有?????????????。
(2)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是(用化学反应方程式表示)?????????????????。
在实验室中,常将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图所示)。
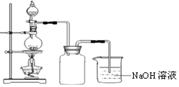
(3)写出烧瓶中发生反应的离子方程式为????????????????????????????????
(4)广口瓶的作用是?????????????????
(5)为符合绿色化学的要求,某研究性学习小组进行如下
设计:将3.2 g铜丝放到45 mL 1.5 mol・L-1的稀硫酸中,控温在50 ℃。加入18 mL 10%的H2O2,反应0.5h后,升温到60 ℃,持续反应1 h后,过滤、蒸发浓缩、减压抽滤等,用少量95%的酒精淋洗后晾干,得CuSO4・5H2O 10.5 g。请回答:
①加热时温度不宜过高的原因是???????????????????????????;
②本实验CuSO4・5H2O的产率为??????????????。
参考答案:⑴? Fe2O3+6H+=2Fe3++3H2O,2Fe3++
本题解析:
试题分析:(1)铁丝表面有铁锈。投入稀H2SO4中发生反应的两种方程式为:Fe2O3+6H+=2Fe3++3H2O;2Fe3++Fe=3Fe2+;Fe+2H+=Fe2++H2↑;(2)为了使灼烧后的氧化铜混合物充分酸溶,在加入稀H2SO4的同时,还通入O2。通入O2的目的是使Cu变为氧化铜,与酸反应得到CuSO4.反应的方程式为:2Cu+O2+2H2SO4=2CuSO4+2H2O 或2Cu+O2=2CuO,CuO+H2SO4=CuSO4+H2O ;(3)在烧瓶中Cu与稀硝酸发生反应的离子方程式为:
本题难度:一般
3、选择题 用16g某饱和一元醇跟足量金属钠完全反应,产生5.6L氢气(标准状况),该醇是
A.甲醇
B.乙醇
C.丙醇
D.丁醇
参考答案:A
本题解析:5.6L氢气(标准状况)是0.25mol,由于2个羟基才能产生1分子氢气,所以该饱和一元醇的物质的量是0.5mol,则其相对分子质量是16÷0.5=30。根据饱和一元醇的通式CnH2n+2O可知,醇是甲醇,答案选A。
本题难度:一般
4、选择题 下列各组金属最合适用氢气或CO把它们从化合物中还原出来的是(???)
A.Ca、Mg
B.Al、Fe
C.Fe、Cu
D.Hg、Ag
参考答案:C
本题解析:在金属活动顺序表中,位于氢后面的金属(如Hg、Ag等),适合用热分解法冶炼;位于氢前面的几种很活泼的金属(如K、Na、Mg、Ca、Al等)适合用电解其熔融盐或氧化物的方法来冶炼;多数金属(如Fe、Cu等)的冶炼可用热还原法。
本题难度:一般
5、选择题 已知将煤进行干馏,可以得到粗苯等物质,将苯与溴水混合,充分振荡后静置,用分液漏斗分出上层液体放置于一试管中,若向其中加入一种试剂,可发生反应并产生白雾.这种试剂是[???? ]
A.浓H2SO4
B.HNO3
C.锌粉
D.铁粉
参考答案:D
本题解析:
本题难度:一般