微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)? A、B、C、D四种元素均属于短周期元素,且原子序数依次增大,A与B能组成 原子数之比为2∶1的化合物X和1∶1的化合物Y,D与B也能组成原子数之比为2:1的化合物M和1:1的化合物Z;1molC单质跟X反应放出0.5mol气体B2,1molD单质跟X反应放出11.2L(标准)气体A2,1molZ化合物跟X反应放出0.5mol气体B2。试回答:
原子数之比为2∶1的化合物X和1∶1的化合物Y,D与B也能组成原子数之比为2:1的化合物M和1:1的化合物Z;1molC单质跟X反应放出0.5mol气体B2,1molD单质跟X反应放出11.2L(标准)气体A2,1molZ化合物跟X反应放出0.5mol气体B2。试回答:
(1)A、B、C、D的元素符号:A?????????B?????????C?????????D??????????
(2)这四种元素形成的四种简单离子的半径大小顺序为____________________;[
(3)这四种元素的原子半径大小顺序为 _________________________________;
(4)C与X反应的化学方程式??????????????????????????????????
(5)Z与X反应的离子方程式??????????????????????????????????
参考答案:
 本题解析:略
本题解析:略
本题难度:一般
2、填空题 (8分)A、B、C等八种物质有如下框图所示转化关系。又知,A是由地壳中含量最多的金属元素形成的单质,C、D、E是常见的由短周期元素形成的气体单质,气体F与气体G相遇产生大量的白烟,H是厨房中必备一种调味盐(部分反应物和生成物及溶剂水已略去)。
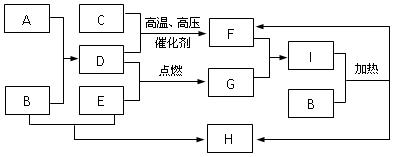
请回答下列问题:
⑴ B的化学式是?????????,F的化学式是??????。
⑵写出D和E反应的化学方程式:???????????????????????????????????。
 ⑶如何检验I中的阳离子????????????????????????????????????????????
⑶如何检验I中的阳离子????????????????????????????????????????????
参考答案:(8分)⑴NaOH? NH3?⑵H2 + Cl2 =(点燃)
本题解析:略
本题难度:简单
3、实验题 有一种无色混合气体,可能含有CH4、NH3、H2、CO、CO2和HCl.进行如下实验:①此混合气体通过浓硫酸,气体体积不变;②再通入澄清石灰水,气体体积变小但无混浊现象;③剩余气体在空气中引燃,燃烧产物不能使无水硫酸铜变色。
(1)根据实验①,可推断混合气体中没有___________________,原因是____________________.
(2)根据实验③,可推断混合气体中没有__________________,原因是___________________.
(3)混合气体中肯定有__________________________________.
(4)上述实验_______________(填“有”或“没有”)不能肯定或否定的气体。若有。则是________________气体。
参考答案:(1)NH3。混合气体可能有的气体中只有NH3能被浓硫酸吸收
本题解析:(1)NH3。混合气体可能有的气体中只有NH3能被浓硫酸吸收;
(2)H2和CH4。H2、CH4燃烧产物中有H2O,而无水CuSO4未变色;
(3)CO、HCl;
(4)有,CO2。
本题难度:简单
4、填空题 (13分)已知M是无色液体,C、H、D是有刺激性气味的气体,且D是单质,E为三原子非极性分子,②是工业上制取F的反应,J为漂白粉的有效成份。(部分反应条件未列出)

请回答下列问题:
(1)E、D、J的化学式分别是?????????、????????、?????????,G的电子式?????
(2)反应④的化学方程式??????????????????????????????????????????????
(3) 简述C的一种用途:???????????????????????????????
(4) A由三种元素组成,1 mol A与M反应可生成1 mol B和2 mol C,则A的化学式是?????????????
(5)漂白粉常用作消毒剂、杀菌剂、漂白剂等。漂白粉是一种混合物,漂白粉质量高低由"有效氯"(过量酸与漂白粉作用生成的氯气的质量与漂白粉的质量比)决定。漂白粉样品2.00克,加水研磨后,转入250毫升容量瓶内,用水稀释至刻度,摇匀后,取出25.0毫升,加入过量的KI溶液和过量的稀硫酸,静置。待漂白粉放出的氯气与KI完全反应后,用0.100摩/升的Na2S2O3标准溶液滴定反应中生成的碘。反应如下:2Na2S2O3+I2=Na2S4O6+2NaI滴定时用去Na2S2O3溶液20.0毫升。计算该漂白粉中有效氯的百分含量。
已知漂白粉与酸的反应为:Ca(ClO)2+CaCl2+2H2SO4=2CaSO4+2Cl2↑+2H2O
参考答案:(10分)
(1)CO2???Cl2
本题解析:略
本题难度:一般
5、填空题 (17分)根据下表部分短周期元素的性质或原子结构,用化学用语回答下列问题。
元素编号
| 元素性质或原子结构
|
R
| 元素所处的周期数、主族序数、原子序数均相等
|
T
| 最外层电子数是次外层电子数的2倍
|
X
| 元素最高正价+7价
|
Y
| 第三周期金属元素中原子半径最小
|
Z
| 常温下单质为双原子分子,其氢化物水溶液呈碱性
(1)写出元素T的原子结构示意图??????????????????;元素Z单质的电子式??????????????????;写出X在周期表中的位置??????????????????????????? ;元素T的最高价氧化物的结构式????????.
(2)探寻物质的性质差异是学习的重要方法之一。上述T、X、Y、Z四 种元素最高价氧化物的水化物的酸性最强的是??????????????????(填化学式),其中化学性质明显不同于其他三种化合物的 种元素最高价氧化物的水化物的酸性最强的是??????????????????(填化学式),其中化学性质明显不同于其他三种化合物的
是??????????????????(填化学式),理由是????????????????????????????????????。
(3)写出R、T、X、三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的化学式???????????????
(4)由表中元素形成的常见物质A、B、C、D、E可发生以下反应:
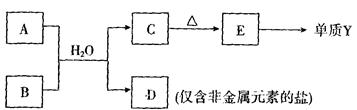
A溶液与B溶液(呈碱性)反应的离子方程式为?????????????????????????????????。
D中含有化学键的类型是?????????????????????,属于??????(填“离子”或“共价”)化合物。
参考答案:
 本题解析:略 本题解析:略
本题难度:一般
|