微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在体积为1L的密闭容器中发生反应2SO2(g)+O2(g) 2SO3(g)。达到平衡后,若采用下列措施一段时间后,能增大逆反应速率的是
2SO3(g)。达到平衡后,若采用下列措施一段时间后,能增大逆反应速率的是
A.体积不变,通入NO
B.增大容器容积
C.体积不变,通入大量O2
D.降低体系温度
参考答案:C
本题解析:
试题分析:NO和氧气反应使氧气浓度降低,平衡左移,SO3浓度减小,故A错误;增大容器容积,SO3浓度减小,故B错误;通入大量O2,平衡右移,SO3浓度增大,故C正确 ;降低温度,正逆反应速率均减小,故D错误。
考点:本题考查化学反应速率。
本题难度:一般
2、选择题 在2A+B?3C+4D反应中,表示该化学反应速率最快的是( )
A.v(A)=0.5mol/(L?s)
B.v(B)=0.3mol/(L?s)
C.v(C)=0.8mol/(L?s)
D.v(D)=1mol/(L?s)
参考答案:在2A+B?3C+4D反应中都换成B的速率减小比较:
本题解析:
本题难度:简单
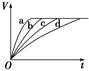
3、选择题 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测得不同时间(t)内产生气体体积(V)的数据如图,根据图示分析实验条件,下列说法中一定不正确的是(??)
组合
| 对应曲线
| c(HCl)/mol・L-1
| 反应温度/℃
| 铁的状态
|
1
| a
| ?
| 30
| 粉末状
|
2
| b
| ?
| 30
| 粉末状
|
3
| c
| 2.5
| ?
| 块状
|
4
| d
| 2.5
| 30
| 块状
?
A.第1组实验中盐酸的浓度大于2.5 mol・L-1
B.第2组实验中盐酸的浓度等于2.5 mol・L-1
C.第3组实验的反应温度低于30 ℃
D.第4组实验的反应速率最慢
参考答案:C
本题解析:由图象可知,反应速率:a>b>c>d,D正确。第1、2两组中反应温度相同,铁的状态相同,前者速率大于后者,说明前者盐酸浓度大。第2、4两组中由于铁的状态不同,所以无法判断盐酸的浓度大小,若前者盐酸的浓度是2.5 mol・L-1,则速率也是前者快,A、B可能正确。第3、4两组中盐酸浓度相同,铁的状态相同,而v(c)>v(d),说明第3组中反应温度比第4组高,C错误。
本题难度:一般
4、选择题 升高温度,下列数据不一定同时增大的是? (?????)
A.化学反应速率v
B.弱电解质的电离平衡常数Ka
C.化学平衡常数K
D.水的离子积常数KW
参考答案:C
本题解析:
试题分析:升高温度,化学反应速率增大,故A一定增大;电离均是吸热过程,故电离平衡常数和水的离子积常数均增大,B、D正确;当正反应为放热反应时,升高温度,平衡向左移动,平衡常数减小,当正反应为吸热反应时,升高温度,平衡向右移动,平衡常数增大,故选C。
本题难度:简单
5、实验题 化学反应速率的变化和化学平衡移动的规律都可以通过实验得出结论,勒夏特列原理也是由实验总结出来的。
(1)将铜片投入到稀硝酸中,开始时产生气泡的速率很慢,随后反 应速率增大,根据你学到的知识分析,反应速率增大的原因是________________ __________________。当进行一段时间后,反应速率又减慢,这次速率减慢的原因是_______________________________。 应速率增大,根据你学到的知识分析,反应速率增大的原因是________________ __________________。当进行一段时间后,反应速率又减慢,这次速率减慢的原因是_______________________________。
(2)丙酮和碘在酸性溶液中发生下列反应:CH3COCH3+I2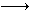 CH3COCH2I+H++I-。25℃时,该反应的速率由下列经验公式决定: CH3COCH2I+H++I-。25℃时,该反应的速率由下列经验公式决定:
υ=k?c(CH3COCH3)?c(H+)[mol/(L?s)]
根据该经验公式,如果c(I2),c(CH3COCH3),c(H+)的起始浓度依次为0.01 mol/L,0.1 mol/L,0.01 mol/L,分析反应速率的变化趋势是_______________ ________________。
(3)在一支试管中先加入30 mL 0.01 mol/L FeCl3溶液,再滴加10 mL 0.01 mol/L KSCN溶液,摇匀。将制得的溶液平均分装于4支试管中,然后分别加入:①FeCl3固体;②KSCN固体;③KCl固体;④H2O。充分振荡后,溶液的颜色基本不变的是________(填序号)。
(4)在50 mL的注射器中吸入40 mL NO2和N2O4的混合气体,在另一同样规格的注射器中吸入40 mL Br2(g),对比两注射器中气体的颜色完全一致。然后都将注射器的活塞慢慢推至20 mL处,发现注射器内气体的颜色变化的现象是___________________________。推测平衡移动是通过观察装入NO2和N2O4的混合气体的注射器内气体的颜色比装入Br2(g)的注射器内气体的颜色_______。
(5)如果要鉴别密封于由两球连通的密闭容器中充满的红棕色气体是NO2和N2O4混合气还是Br2(g),可以____________________。
参考答案:(1)该反应是放热反应(1分)。随着反应的进行,硝酸的浓度减
本题解析:略
本题难度:一般
|