微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (7分)有一无色透明溶液,,可能含有Na+、K+、Fe2+、Ba2+、NO3-、SO32-、SO42-离子中的若干种,依次进行下列实验,观察到的现象如下。
①取少量该溶液,滴加氯水,氯水褪色。
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热, 有无色气体产生,后在空气中又变成红棕色
③用洁净的铂丝蘸取该溶液,在酒精灯火焰上灼烧,火焰呈黄色
④取少量该溶液,加入足量BaCl2溶液,产生白色沉淀,再加足量稀硝酸,沉淀不溶解。
根据上述实验现象判断:
(1)溶液中肯定存在的离子是???????????????????????????????。
(2)溶液中可能存在的离子是???????????????????????????????。
(3)为进一步确定可能存在的离子,应该补充的实验是??????????????????????????。
参考答案:(1)Na+、NO3-、SO32-(2分)(若少一个离子扣1
本题解析:因为是无色透明溶液,属于亚铁离子没有。滴加氯水,氯水褪色,说明含有还原性离子,因此一定含有SO32-。因为Ba2+和SO32-不能大量共存,所以一定没有Ba2+。有无色气体产生,后在空气中又变成红棕色,所以气体是NO,被氧化生成NO2,因此实验②说明含有NO3-。实验③说明含有Na+。实验④中的白色沉淀是硫酸钡,但由于前面的实验中SO32-被氧化生成了SO42-,实验无法证明是否含有SO42-。
本题难度:简单
2、填空题 (8分)某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等离子,进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀生成。
(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
(4)另取少量步骤(3)中的滤液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有?????????????????????离子;
一定不含有?????????????离子;还有_________________离子不能确定是否存在,要检验这些离子的实验方法是????????????????,操作是______________________________________________。
参考答案:Ag+、Ba2+、NH4+?;Fe3+;K+??;焰色反应;
本题解析:加入过量的稀盐酸,有白色沉淀生成,说明含有银离子。根据(2)可知溶液中含有钡离子。根据(3)可知溶液中没有铁离子。根据(4)可知气体是氨气,说明含有NH4+。所以待测液中一定含有Ag+、Ba2+、NH4+;一定不含有Fe3+;可能含有K+。钾离子的检验,可以用焰色反应,即用铂丝沾取溶液在酒精灯上灼烧并透过蓝色钴玻璃观察火焰颜色。
本题难度:一般
3、选择题 下列说法正确的是???????????????????????????????????????????????????????????????????????????????????????(???)
A.镁与极稀硝酸反应生成硝酸铵的离子方程式为:
4Mg+6H++NO3- =4Mg2++NH4++3H2O
B.25℃时,将20 mL 0.1mol・L-1H2SO4溶液和30 mL 0.15mol・L-1NaOH溶液混合,若混合后溶液体积不变,则混合溶液的pH为11
C.将10 mL 0.1 mol・L-1KAI(SO4)2溶液和10 mL0.2 mol・L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物质的量之比为1:2
D.浓度均为0.1 mol・L-1的醋酸和CH3COONa溶液等体积混合,溶液中有下列关系:
c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
参考答案:D
本题解析:略
本题难度:一般
4、填空题 X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲由X、Z、Q三种元素组成,常温下0.1 mol/L甲溶液的pH=13。工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成。请回答下列问题:
(1)Q的原子结构示意图为________。
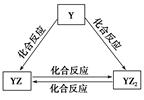
(2)Y元素的单质能发生如图所示的转化,则Y元素为________(填元素符号)。
在甲溶液中通入足量YZ2气体,所得溶液呈碱性,原因是__________________(用离子方程式和必要的文字说明)。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为______________________________________________________________________________;
②Q、W两种元素金属性的强弱为Q________W(填“<”或“>”),下列表述中能证明这一事实的是________(填序号)。
a.Q单质的熔点比W单质的低
b.Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
c.W的原子序数大
参考答案:(1) 本题解析:(1)化合物甲由X、Z、Q三种元素组成,常温下0.1 mol/L甲溶液的pH=13,说明甲溶液呈碱性,且为强碱,因为其完全电离,又因为X、Z、Q均为短周期元素,且原子序数依次增大,故确定为NaOH。则X为H、Z为O、Q为Na。(2)因为Y在元素周期表中介于H和O之间,又根据框图分析,Y可以与氧气反应分别生成YO和YO2,故Y可能为碳元素或氮元素,但框图中指明YO2可以发生化合反应生成YO,所以确定Y为碳元素。向氢氧化钠溶液中通入足量二氧化碳可得到碳酸氢钠溶液,碳酸氢根离子的水解能力大于其电离能力,故溶液呈
本题解析:(1)化合物甲由X、Z、Q三种元素组成,常温下0.1 mol/L甲溶液的pH=13,说明甲溶液呈碱性,且为强碱,因为其完全电离,又因为X、Z、Q均为短周期元素,且原子序数依次增大,故确定为NaOH。则X为H、Z为O、Q为Na。(2)因为Y在元素周期表中介于H和O之间,又根据框图分析,Y可以与氧气反应分别生成YO和YO2,故Y可能为碳元素或氮元素,但框图中指明YO2可以发生化合反应生成YO,所以确定Y为碳元素。向氢氧化钠溶液中通入足量二氧化碳可得到碳酸氢钠溶液,碳酸氢根离子的水解能力大于其电离能力,故溶液呈
本题难度:一般
5、填空题 (6分)有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰。
由上述现象推断:该混合物中一定含有????????;一定不含有???????;可能含有???????
参考答案:(6分) Na2CO3?、Na2SO4、Ba(NO3)2?;
本题解析:粉末溶于水得无色溶液和白色沉淀,说明一定没有CuCl2,一定含有Ba(NO3)2;在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体,说明生成的白色沉淀是碳酸钡和硫酸钡;取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰,说明一定没有K2CO3,所以一定含有Na2CO3?、Na2SO4,而氯化钠是不能确定的。
本题难度:一般