微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 等质量的下列物质中,所含分子数最少的是
A.Cl2
B.HCl
C.Br2
D.HBr
参考答案:C
本题解析:分析:根据n=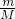 =
= 计算,物质的物质的量越小,分子数越小.
计算,物质的物质的量越小,分子数越小.
解答:假设质量都为mg,则
A.N(Cl2)=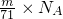 ;
;
B.N(HCl)= ;
;
C.N(Br2)=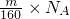 ;
;
D.N(HBr)= ,
,
则所含分子数最少的是Br2,
故选C.
点评:本题考查物质的量的计算,本题也可根据n=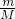 =
= 直接得出分子数与摩尔质量的关系进行判断.
直接得出分子数与摩尔质量的关系进行判断.
本题难度:困难
2、选择题 下列关于燃烧的说法不正确的是
A.都是化学变化
B.都是氧化反应
C.都是放热反应
D.都是化合反应
参考答案:D
本题解析:试题分析:本题是对燃烧概念的考查。对于燃烧反应,并不一定都是化合反应。化合反应的定义是:由两种或两种以上物质反应生成一种物质的化学反应。实例:蜡烛的燃烧,其产物是二氧化碳和水。由化合反应的定义可得,蜡烛的燃烧反应并不是化合反应。故答案选D。
考点:燃烧的定义;化合反应
点评:本题是以“燃烧”为载体,结合考查了四大反应类型中的化合反应。其解题要求在于明确基本的概念。燃烧:通常的燃烧是指可燃物与氧气发生的一种发光、放热的剧烈的氧化反应。
本题难度:一般
3、选择题 物理量的符号及其单位都正确的是
A.阿伏加德罗常数:NA,mol
B.摩尔质量:M,g?mol-1
C.气体摩尔体积:Vm,mol?L-1
D.物质的量浓度::C,L 91exam.org?moL-1
参考答案:B
本题解析:分析:根据各物理量的定义解答该题.
解答:A、阿伏加德罗常数0.012kg12C中所含的原子数目叫做阿伏加德罗常数,阿伏加德罗常数的符号为NA,阿伏加德罗常的近似值为:6.02×1023/mol,故A错误;
B、摩尔质量为单位物质的量的物质的质量,符号为M,单位是g?mol-1,故B正确;
C、气体摩尔体积为一定条件下的单位物质的量的气体的体积,表达式为Vm= ,符号为Vm,单位为L/mol,故C错误;
,符号为Vm,单位为L/mol,故C错误;
D、物质的量浓度为单位体积溶液含有溶质的物质的量,表达式为=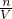 ,符号为C,单位为mol/L,故D错误.
,符号为C,单位为mol/L,故D错误.
故选B.
点评:本题考查常见物理量的了解,题目难度不大,注意基础知识的积累.
本题难度:困难
4、选择题 法国化学家拉瓦锡对近代化学的最大贡献是
A.最早使用天平研究化学
B.最早提出空气是由O2和N2组成的结论
C.建立燃烧现象的氧化学说
D.能用加热HgO的方法制取O2
参考答案:C
本题解析:题中四项都是法国拉瓦锡的贡献.拉瓦锡的最大贡献是建立了燃烧现象的氧化学说,纠正了化学科学上的“燃素说”.
本题难度:一般
5、选择题 NA代表阿伏加德罗常数的值,下列说法正确的是
A.常温常压下,1mol水含有NA个H+和NA个OH-离子
B.在通常状况下,22.4?LH2和4?gHe均含有NA个分子
C.8.0?g?Cu2S和CuO的混合物中约含有铜原子数为0.1NA
D.常温常压下,0.1mol铁与0.1molCl2充分反应,转移的电子数约为0.3NA
参考答案:C
本题解析:分析:A、水是弱电解质存在电离平衡;
B、22.4?LH2在通常状况下不是1nol;
C、质量换算物质的量分别计算物质含有的铜原子比较;
D、等物质的量铁和氯气反应生成三氯化铁,结合化学方程式的过量计算判断;
解答:A、水是弱电解质不能完全电离,故A错误;
B、在通常状况下,22.4?LH2物质的量不是1mol,故B错误;
C、8.0?g?若全是Cu2S含铜原子= =0.1mol;8.0?g?若全是CuO含铜原子=
=0.1mol;8.0?g?若全是CuO含铜原子=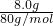 =0.1mol;所以8.0?g?Cu2S和CuO的混合物中约含有铜原子数为0.1NA,故C正确;
=0.1mol;所以8.0?g?Cu2S和CuO的混合物中约含有铜原子数为0.1NA,故C正确;
D、0.1mol铁与0.1molCl2充分反应铁有剩余,转移电子数用全反应的氯气计算为0.2mmol,故D错误;
故选C.
点评:本题考查了弱电解质的电离平衡,气体摩尔体积的条件应用,质量换算物质的量计算微粒数,氧化还原反应的过量计算电子数的计算.
本题难度:一般