微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的1/6;B元素原子核外电子数比A元素原子核外电子数多1;C-离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层的2倍。请填写下列空格:
(1)请写出A的元素符号???????;
(2)C的一价阴离子的结构示意图????????????????????;
B的原子的结构示意图????????????????????;
(3)A、B两元素相比较,A元素的金属性较强,可以验证该结论的实验是(??)。
A.将这两种元素的块状单质分别放入冷水中
B.将这两种元素的单质分别和同浓度的盐酸反应
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞试液???
D.比较这两种元素的气态氢化物的热稳定性
参考答案:(1)Mg??? (2) 本题解析:
本题解析:
本题难度:一般
2、选择题 运用元素周期律分析下面的推断,其中错误的是 ( )
A.砹(85号元素)是一种有色固体,HAt应该不稳定,且AgAt是有色难溶于水固体
B.铍(Be)是一种金属,它的氧化物的水化物可能具有两性
C.硫酸锶(SrSO4)是难溶于水和盐酸的的白色固体
D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列各组粒子按氧化性由弱到强,半径由大到小顺序排列的是()
A.O、Cl、S、P
B.K+、Mg2+、Al3+、H+
C.Ca2+、Mg2+、Al3+、K+
D.I-、Br-、Cl-、F-
参考答案:B
本题解析:
本题难度:一般
4、填空题 元素周期表反映了元素性质的周期性变化规律。请根据短周期元素在周期表中的位置、结构和相关性质,回答下列问题:
(1)第VIA族元素形成的氢化物中沸点最高的是____________(用分子式表示),原因是____________________,该分子的空间构型为______________。
(2)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如表1所示,其中E的化学式为??????;第三周期元素单质的熔点(℃)变化如图a所示,其中h的元素符号为????????????。???????????????(表1)
氢化物
| A
| B
| HF
| D
| E
|
沸点/℃
| 1317
| 100
| 19.5
| 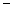 33.35 33.35
| 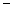 164 164
(3)第二、第三周期的某些元素能形成单质甲和化合物乙,它们具有图b所示的结构单元,甲和乙的晶体类型相同,甲的某种同素异形体与乙在高温时能发生置换反应生成h的单质和CO。若该反应生成的h的单质含有1 mol共价键,则参加反应的乙的质量为_______________g。
(4)碳元素的某种单质具有平面层状结构,该单质的名称为__________;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为???????????????。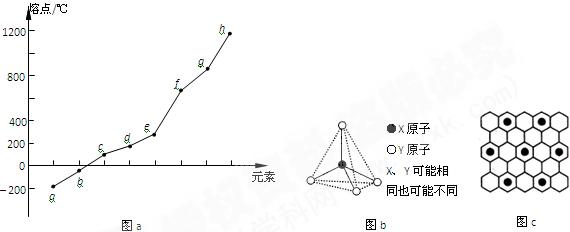
参考答案:(1)H2O? H2O分子间可以形成氢键?角型或折线型
本题解析:
本题难度:简单
5、选择题 已知X、Y、Z元素的原子具有相同的电子层数,且原子序数依次增大,其最高价氧化物对应水化物酸性依次增强,则下列判断正确的是 (??? )
A.最高化合价按X、Y、Z的顺序减小
B.阴离子的还原性按X、Y、Z顺序增强
C.单质的氧化性按X、Y、Z顺序增强
D.氢化物的稳定性按X、Y、Z顺序减小
参考答案:
C
本题解析:
本题难度:简单
|