微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 水的电离平衡曲线如下图所示。下列说法正确的是????????????? ( )
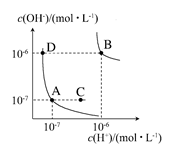
A.图中对应点的温度关系为A>B
B.水的电离常数KW数值大小关系为B>D
C.温度不变,加入少量NaOH可使溶液从C点变到A点
D.在B点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显酸性
参考答案:B
本题解析:温度越高KW越大,故A错误;B点及其所在曲线上的点表示的KW为1×10-12,而A点及其所在曲线上的点表示的KW为1×10-14,故B正确;温度不变,KW不变,加入少量NaOH也不能使溶液从C点变到A点,只有改变温度方可实现,C错误。
本题难度:一般
2、实验题 用50mL 0.50mol・L-1盐酸与50mL 0.55mol・L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
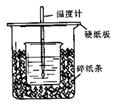
(1)从实验装置上看,图中尚缺少的一种玻璃仪器的名称是???????????????????????。
(2)烧杯间填满碎纸条的作用是??????????????????????????。
(3)大烧杯上如不盖硬纸板,求得的中和热数值??????????(填“偏大、偏小、无影响”)
(4)如果用60mL 0.50mol・L-1盐酸与50mL 0.55mol・L-1NaOH溶液进行反应,与上述实验相比,所放出的热量????????(填“相等、不相等”),所求中和热?????????(填“相等、不相等”)。
参考答案:(1)环形玻璃搅拌棒(2)减少热量散失(3)偏小(4)不相等
本题解析:考查中和热的测定,主要是注意热量的损耗,尽量减小误差。
(4)参加反应的物质的量不同,放出的热量必然不同,但经折算为中和热后应相等。
本题难度:一般
3、选择题 下列叙述正确的是(????)
A.95 ℃纯水的pH<7,说明加热可导致水呈酸性
B.pH = 3的醋酸溶液,稀释至10倍后pH<4
C.0.2 mol・L-1的盐酸,与等体积水混合后pH = 2
D.pH = 3的醋酸溶液,与pH = 11的氢氧化钠溶液等体积混合后pH = 7
参考答案:B
本题解析:
试题分析:A不正确,任何水中都是显中性的;醋酸存在电离平衡,稀释促进电离,所以氢离子的物质的量增加,B正确;C不正确,因为混合后溶液的体积不是原来的2倍;D不正确,反应后醋酸过量,溶液显酸性,答案选B。
点评:在判断酸碱中和后溶液的酸碱性时,不能首先考虑生成的盐是否水解,而是要先判断酸或碱的过量问题。只有当酸和碱恰好反应时,才能考虑生成的盐是否水解。
本题难度:一般
4、选择题 下列说法中正确的是[???? ]
A.25℃、101kPa时,1mol碳完全燃烧生成CO2和水时所放出的热量为碳的燃烧热
B.已知2CO(g)+O2(g)=2CO2(g);△H=-566 kJ/mol,则CO的燃烧热为566 kJ/mol
C.25℃、101KPa时,1g甲醇完全燃烧生成CO2和液态水,同时放出22.68kJ热量,则甲醇的燃烧热△H=-725.8kJ/mol
D.N2(g)+O2(g)=2NO(g); △H=+90.4 kJ/mol,故N2的燃烧热为90.4 kJ/mol
参考答案:C
本题解析:
本题难度:简单
5、填空题 (6分)25℃时,体积为Va、pH=α的某一元强酸溶液与体积为Vb、pH=b的某一元强碱溶液混合后恰好完全反应。若Va>Vb,且α=0.4b,请填写下列空白:
(1)a可否等于2?(填“可”或“否”)__________。
(2)a可否等于4?(填“可”或“否”)__________。
(3)a的取值范围是_____________________。?
参考答案: 本题解析:略
本题解析:略
本题难度:一般