A.金属钠失火,用泡沫灭火器扑灭
B.用瓷坩埚熔融氢氧化钠或碳酸钠固体
C.用滴有酚酞的水做喷泉实验,只验证了氨气的溶解性
D.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼
参考答案:ABC
本题解析:试题分析:
本题难度:简单
2、填空题 (10分)某同学用18 mol/L的浓硫酸配制200mL 0.9mol/L的稀硫酸,并进行有关实验。请回答下列问题:
(1)需要量取浓硫酸? ??mL(准确到小数点后一位)。
(2)配制该稀硫酸时使用的仪器除量筒、烧杯、200mL容量瓶外,还必须用到的仪器有? ??、? ??等。
(3)容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧。有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是(?? )
A.可以按此建议改进,便于使用容量瓶
B.不能按此建议改进,因为会降低容量瓶的精确度
C.如果加粗瓶颈,可将原来刻在容量瓶瓶颈上的刻度线改刻在容量瓶的瓶身上
D.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响
(4)在配制过程中,下列因素对所配制的稀硫酸的物质的量浓度有何影响?
若容量瓶未干燥即用来配制溶液,则所得溶液浓度? 0.9 mol・L-1(填“大于”、“等于”或“小于”,下同);若定容时俯视刻度线,则所得溶液浓度? 0.9 mol・L-1。
参考答案:(共10分) (1)10.0? (2分)
(2)玻璃
本题解析:
试题分析:(1)在浓硫酸的稀释过程中,溶质是不变的,所以需要量取浓硫酸的体积是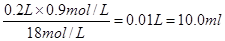 。 。
(2)稀释浓硫酸、向容量瓶中转移硫酸时都需要玻璃棒。另外定容时还需要胶头滴管。
(3)根据容量瓶的结构可知,瓶颈越粗,精确度越低,所以该建议不可取,答案选B。
(4)根据n=c・V可知,如果容量瓶没有干燥,则溶质的溶液的体积不受影响,浓度不变;如果定容时俯视刻度线,则所得溶液的体积偏少,浓度偏高。
点评:该题是高考中的常见题型,属于中等难度的试题。试题侧重考查学生的基础知识,兼顾能力的考查。该题的难度在于误差分析,配制一定物质的量浓度溶液的实验是中学化学中一个重要的定量实验,实验过程中引起溶液浓度存在误差的因素有很多。从大的方面讲,一是由实验过程中的不规范操作引起的;二是由仪器或药品等系统原因引起的。由于引起误差的原因复杂,所以误差分析就成为高考化学实验中的一个难点。
本题难度:一般
3、实验题 某学生用0.1000 mol・L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液
B.用标准氢氧化钠溶液润洗滴定管2-3次
C.把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处
E.调节液面至“0”或“0”刻度以下,记下读数,为3.10mL
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。回答下列问题:

(1)正确的操作顺序是:B、????????????????????、F(填序号);
(2)上述B步骤操作的目的是???????????????????????????????????????;
(3)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响??
是??????????????????????????????(填“偏大”或“偏小”或“无影响”);
(4)判断到达滴定终点的实验现象是???????????????????????;
(5)若滴定结束时,滴定管液面如图所示,则终点读数为??????????????mL。
(6)根据读数计算出该待测液的浓度为????????????????????????????????????????。
参考答案:(1)D C E A???(2)防止滴定管内壁附着的水将标准
本题解析:
试题分析:(1)用0.1000 mol・L-1标准氢氧化钠溶液滴定未知浓度的盐酸溶液时,其正确的操作为用标准氢氧化钠溶液润洗滴定管2-3次,取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2-3mL处,把盛有标准氢氧化钠溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液,调节液面至“0”或“0”刻度以下,记下读数,为3.10mL,取20.00 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2-3滴酚酞试液,把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管的读数。所以答案为D C E A;(2)中,B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差;(3)中,若先用待测溶液润洗锥形瓶,则会使测定结果偏大;(4)中,到达滴定终点的实验现象是溶液由无色变为浅红色,且半分钟内不褪色;(5)中,终点读数为21.10,注意小数点的精确位数;(6)中,根据cv=c1v1
可以得到,0.1000×(21.10-3.10)=20c1,解得c1为0.09000mol・L-1。
点评:该题考查了如何配置溶液以及酸碱滴定的相关知识,难度不大,解答该题要注意仪器的读数所精确的位数。
本题难度:一般
4、选择题 下列有关物质制备的说法错误的是
A.实验室制备O2可用H2O2和MnO2为原料方便制得
B.人类社会发展史,也是人类金属冶炼史,由于化学工艺所限不活泼金属往往人类先发现并制得,随着化学发展,活泼金属逐渐被人们发现并制得,如金早于铜,铜早于铁,铁早于铝,铝早于钠。
C.工业制备镁采用电解熔融氯化镁的方法
D.工业采用电解饱和食盐水的方法制备氯气。
参考答案:B
本题解析:略
本题难度:一般
5、实验题 3位同学设计了下列3个实验方案以验证某无色气体中既含有SO2,又含有CO2。
方案1:将无色气体通入酸性KMnO4溶液,KMnO4溶液褪色,反应后气体通入石灰水,石灰水变浑浊。即可证原无色气体中含有SO2,又含有CO2。
方案2:将无色气体通入溴水,溴水褪色又应后气体通入石灰水,石灰水变浑浊,证明原无色气体中既含有 SO2,又含有CO2。
方案3:将无色气体通入品红试液后再依次通入酸化KMnO4溶液、品红溶液,最后通入澄清的石灰水。结果品红试液褪色、KMnO4溶液颜色变浅品红试液不褪色,石灰水变浑浊,证明原无色气体既含有SO2,又含有CO2。
试回答上述3个方案中,能证明原无色气体中既有SO2,又有CO2的方案是:???????????????简述其理由是???????????????????。
参考答案:符合上述实验程序的应是方案3。检验SO2存在→除SO2→证明
本题解析:分析时一要考虑SO2与CO2的共性是均能使澄清石灰水变浑,二要考虑到二者的区别,SO2具有还原性,并能使品红褪色,CO2不具备这些性质。三要考虑能使酸性KMnO4溶液、溴水褪色的物质不仅有SO2,还有H2S、C2H4、C2H2等。因此证明既有SO2又有CO2的实验程序一般应为:检验SO2存在→除SO2→证明SO2不存在→证明CO2存在。
本题难度:简单
|