微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是
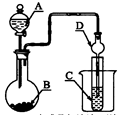
A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液不褪色
B.若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色
D.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀
参考答案:C
本题解析:
试题分析:A、二氧化锰和浓盐酸反应需要加热,该装置没有加热,不能产生氯气,则C中品红溶液不褪色,正确;B、醋酸和贝壳的主要成分碳酸钙反应生成二氧化碳,则C中澄清石灰水变浑浊,正确;C、浓硫酸和亚硫酸钠反应生成二氧化硫,二氧化硫有漂白性,但不能使酸碱指示剂褪色,则C中溶液变红,错误; D、浓氨水和生石灰混合生成氨气,氨气和氯化铝反应生成氢氧化铝,虽然氢氧化铝是两性氢氧化物,但氢氧化铝不和氨水反应,则C中产生白色沉淀,正确。
本题难度:一般
2、选择题 右图是制取和收集某气体的实验装置,该装置可用于
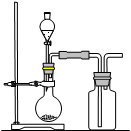
A.用浓硫酸和氯化钠反应制取HCl
B.用浓氨水和生石灰反应制取NH3
C.用双氧水与二氧化锰反应制取O2
D.用饱和食盐水和电石反应制取C2H2
参考答案:C
本题解析:
试题分析:根据装置图可知,该反应适合于制备不需要加热、且密度大于空气的气体。选项AB都需要加热,C正确;D中乙炔的密度小于空气的,不正确,答案选C。
点评:该题主要是考查学生对常见气体制备原理以及收集方法的了解程度,属于基础性试题的检验,难度不大。该题的关键是记住气体的制备原理和气体的性质,然后结合题意灵活运用即可。
本题难度:一般
3、选择题 用氢氧化钠固体配制0.10mol/L的氢氧化钠溶液,下列说法错误的是
A.定容时俯视,会造成浓度偏高
B.转移时不慎将转移液溅出,会造成浓度偏低
C.称量时托盘上要垫上干净的称量纸
D.定容摇匀后发现液面下降,不应继续加水
参考答案:C
本题解析:
试题分析:C项:氢氧化钠易潮解,会留在纸上,应在烧杯中称量,故错。故选C。
点评:本题考查的是配置配置一定物质的量浓度的知识,难度不大,注意基础知识的掌握和应用。
本题难度:简单
4、选择题 实验室中某些气体的制取、除杂及收集装置如图所示。仅用此装置和表中提供的物质完成相关实验,最合理的是
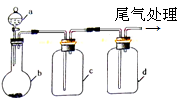
选项
| a中物质
| b中物质
| c中物质
| d中收集的气体
|
A
| 浓氨水
| CaO
| 浓H2SO4
| NH3
|
B
| 浓硫酸
| Na2SO3
| 浓H2SO4
| SO2
|
C
| 饱和食盐水
| 电石
| CuSO4溶液
| CH≡CH
|
D
| 浓盐酸
| MnO2
| 饱和NaCl溶液
| Cl2
?
参考答案:B
本题解析:
试题分析:A项中浓H2SO4吸收NH3。C项中CH≡CH的相对分子质量是26,不能用向上排气法;D项中发生装置需要加热。
本题难度:一般
5、填空题 (12分)手持技术又称掌上技术,是由数据采集器、传感器和配套的软件成
的定量采集各种常见数据并能与计算机连接的实验技术系统。某研究小组利用手持技术,获得8.34gFeS04・7H20样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。
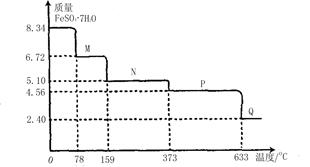
请回答下列问题:
(1)试确定78℃时固体物质M的化学式:?????????????。
(2)取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成且两种气体的组成元素相同,摩尔质量相差16,写出该反应的化学方程式????????????。
(3)某兴趣小组用如图所示装置设计实验,验证(2)中生成的气态物质,并测定已分解的P的质量(不考虑装置内空气的影响)。
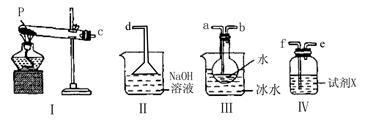
①试剂X的名称是?????????????。
②按气流方向连接各仪器,用字母表示接口的连接顺序:c????????????。
③充分反应后,利用装置Ⅲ中圆底烧瓶内混合物测定已分解的P的质量,其操作步骤为:第一步:向圆底烧瓶中逐滴加入氯化钡溶液,直至沉淀完全;第二步:过滤混合物,在过滤器上将沉淀洗净后,烘干并冷却至室温,称重。第三步:继续烘干、冷却并称量直至连续两次 称量的质量差不超过0.1g为止。若最终得到沉淀的质量为Wg,则已分解的P的质量为?????????????????(填计算式)。
④上述测得P的质量比实际分解质量要小,原因是??????????????。
参考答案:(1)FeS04・4H20?(2)2FeSO4![]()
本题解析:
试题分析:(1)8.34gFeS04・7H20的物质的量是8.34g÷278g/mol=0.03mol,78℃是固体质量减少了8.34g-6.72g=1.62g,即相当于水的物质的量是1.62g÷18g/mol=0.09mol,所以固体中含有的结晶水是0.03mol×7-0.09mol=0.12mol,则化合物中含有的水分子个数是0.12mol÷0.03mol=4,则化学式是FeS04・4H20。
(2)固体加热到373℃时固体质量减少了8.34g-4.56g=3.78g,即相当于水的物质的量是3.78g÷18g/mol=0.21mol,这说明此时水已经完全失去。又因为两种气体的组成元素相同,摩尔质量相差16,所以该物质是二氧化硫和三氧化硫,因此反应的化学方程式是2FeSO4 Fe2O3+SO2↑+SO3↑。 Fe2O3+SO2↑+SO3↑。
(3)①二氧化硫具有漂白性和还原性,所以检验二氧化硫可以用品红溶液或溴水或酸性高锰酸钾溶液。
②三氧化硫溶于水生成硫酸,所以首先要通过冷却水得到三氧化硫,又因为二氧化硫是大气污染物,需要尾气处理,所以正确的顺序是c a a b b f f e e d。 d。
③根据题意最终得到的白色沉淀是硫酸钡,由于生成的硫酸来自于三氧化硫,所以根据S原子守恒可知,分解的硫酸亚铁的质量是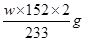 。 。
④由于生成的三氧化硫并没有完全被吸收,导致生成的硫酸钡质量减少,所以测得P的质量比实际分解质量要小。2的检验、三氧化硫的分离等
点评:固体是高考中的常见题型,属于较难的实验题。试题既有定性的分析,也有定量的计算,学生不易得分。本题用图表表述化学过程或呈现背景信息是化学常用的表达方式。图表往往拥有较大的信息存储量,能够很全面地考查学生分析、比较、概括、归纳问题的能力。
本题难度:一般
|