微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 如图所示,B中活塞可以自由滑动。A、B中均有1mol X、1mol Y,起始时,V(A)=V(B)=a L。关闭K,相同温度下,两容器中同时发生反应:2X(g)+2Y(g) Z(g)+2W(g)? ΔH<0,达到平衡(Ⅰ)时,V(B)=0.8a L。
Z(g)+2W(g)? ΔH<0,达到平衡(Ⅰ)时,V(B)=0.8a L。
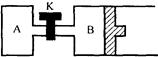
(1)达到平衡所需的时间:A?????????B。(填“>”、“<”、或“=”,下同)
(2)W的百分含量:A ???????????B。
(3)B中X的转化率为?????????????。
(4)打开K,重新达平衡(Ⅱ)时,B的体积为??????L(用含a的式子表示,连通管体积忽略不计)。
参考答案:(1)>?;?
(2)< ;
(3
本题解析:
试题分析:(1)因为B中活塞可以移动,生成物的体积比反应物的体积小,随着反应的进行,活塞会向左移动,使B中的体积变小,与A比较,相当于浓度提高,所以需要的时间减少;
(2)随着活塞不断向左移动,相当于不断提高了反应物的浓度,所以平衡向右移动,增大生成物的量;
(3)当V(B)=0.8a L,B的体积减少了0.2aL,则消耗了0.4aL的X,因为原来有0.5aL的X,所以转化率为80%;
(4)当打开K后,A将达到与未打开K时B同样的平衡,体积将减少为0.2AL,所以活塞将继续向左移动,B中体积变为0.2AL.
本题难度:一般
2、填空题 (10分)在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g)??△H <0
2NH3(g)??△H <0
(1)该反应450℃的平衡常数?????500℃时的平衡常数(填“>”、“<”或“=”);
(2)下列描述中能说明上述反应已达平衡的是?????????????????????
a.3v正(H2)=2v逆(NH3)?????? b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度 不随时间而变化?? d.容器中气体的分子总数不随时间而变化
不随时间而变化?? d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol
计算从反应开始到平衡时,平均反应速率v(N2)为????????mol/(L・min)
(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:???? ??????????????;
(5)第5分钟末,保持其它条件不变, 若继续通入0.2 mol的N2和0.6 mol的H2,
则平衡???????????????移动(填“向正反应方向”“向逆反应方向”或“不”)。
参考答案:(每空2分,共10分)(1)>??????????(2)b
本题解析:略
本题难度:一般
3、选择题 密闭容器中的可逆反应3A(g)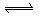 3 B+C?? ΔH="+890" kJ/mol(A的式量为120)随着温度升高,容器中气体相对平均分子质量减小,则下列判断正确的是( ).
3 B+C?? ΔH="+890" kJ/mol(A的式量为120)随着温度升高,容器中气体相对平均分子质量减小,则下列判断正确的是( ).
A.若C为固体,则B一定是气体
B.B和C一定都是气体
C.若起始时往容器中投入18 g A,则反应吸收的热量为44.5 kJ
D.若起始时往容器中投入18 g A,则反应放出的热量为44.5 kJ
参考答案:A
本题解析:略
本题难度:一般
4、选择题 mA(气) + nB(气) pC(气) + qQ(气)当m、n、p、q为任意整数时,下列情况一定是平衡状态的是:
pC(气) + qQ(气)当m、n、p、q为任意整数时,下列情况一定是平衡状态的是:
体系的压强不再改变
体系的温度不再改变
各组分的浓度不再改变
各组分的质量分数不再改变
反应速率Va:Vb:Vc:Vd=m:n:p:q
单位时间内m mol A断键反应,同时p mol C也断键反应
A.③④⑤⑥
B.②③④⑥
C.①③④⑤
D.①③④⑥
参考答案:B
本题解析:
试题分析:①若反应前后气体的体积发生不变,体系的压强不再改变说明到达平衡,若反应前后气体的物质的量不变,体系的压强自始至终不变,体系的压强不再改变不能说明到达平衡,故①错误;②随反应进行体系的温度发生变化,绝热体系的温度不再改变说明到达平衡,故②正确;??③随反应进行各组分的浓度发生不变,各组分的浓度不再改变说明到达平衡,故③正确;④随反应进行各组分的质量分数发生不变,各组分的质量分数不再改变说明到达平衡,故④正确;⑤反应速率自始至终都按vA:vB:vC:vD=m:n:p:q,不能说明到达平衡,故⑤错误;⑥A断键表示正反应速率,C断键表示逆反应速率,单位时间内m?molA断键反应,同时生成pmolC,C的断键与成键相等,说明到达平衡,故⑥正确。
本题难度:一般
5、选择题 可逆反应
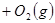

 从正方向开始,并达到了平衡,此时
从正方向开始,并达到了平衡,此时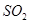 和
和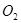 的物质的量之比为2:1,若采取某种措施,导致
的物质的量之比为2:1,若采取某种措施,导致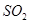 和
和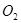 又消耗了一些,并再次达到平衡,下列说法正确的是
又消耗了一些,并再次达到平衡,下列说法正确的是
A.新平衡体系中,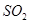 和
和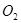 物质的量之比仍为2:1
物质的量之比仍为2:1
B.平衡向正反应方向移动,原因是正反应速率增大,逆反应速率减小
C.新平衡体系与旧平衡体系比较,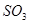 的浓度肯定增大
的浓度肯定增大
D.若所采取的措施是缩小容器的容积,则新旧平衡中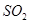 和
和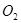 的转化率之比都是1:1
的转化率之比都是1:1
参考答案:D
本题解析:A.若通过增大反应物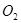 的浓度导致
的浓度导致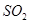 和
和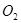 又消耗了一些,则新平衡体系中
又消耗了一些,则新平衡体系中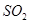 和
和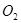 物质的量之比就不是2:1。B. 平衡向正反应方向移动,是因为正反应速率大于逆反应速率。C.如果通过减小
物质的量之比就不是2:1。B. 平衡向正反应方向移动,是因为正反应速率大于逆反应速率。C.如果通过减小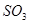 的浓度导致
的浓度导致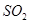 和
和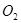 又消耗了一些,则新平衡时
又消耗了一些,则新平衡时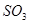 的浓度比原平衡小
的浓度比原平衡小
本题难度:一般