微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在标准状况下,O2和CO2的混合气体共6.72L,其质量为11.4g,则混合气体中氧气的质量分数是????????????????????????????????????????????????????????(???)
A.21%
B.78%
C.50%
D.42.1%
参考答案:D
本题解析:
试题分析:混合气体体积为6.72L,则混合气体的物质的量=6.72/22.4=0.3mol,则设氧气的物质的量为X,有X×32+(0.3-X) ×44=11.4,计算可得X=0.15,则氧气的质量=0.15×32=4.8g,质量分数为4.8/11.4×100%=42.1%。
点评:本题涉及到了混合气体的物质的量计算,利用的还是根据已知条件来找条件,另外还要用到一条规律,不论是混合气体还是纯气体,只要在标况下,体积都是22.4L。
本题难度:一般
2、选择题 PM2.5是指直径小于等于2.5 是悬浮颗粒物,其主要来源为燃煤、机动车尾气等。某实验小组将PM2.5样本用蒸馏水处理制成待测试样。测得该试样呈酸性,其各离子浓度如下表,根据表中数据可知该溶液PH为
是悬浮颗粒物,其主要来源为燃煤、机动车尾气等。某实验小组将PM2.5样本用蒸馏水处理制成待测试样。测得该试样呈酸性,其各离子浓度如下表,根据表中数据可知该溶液PH为
离子
| K+
| Na+
| NH4十
| 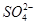
| 
| C1―
|
浓度/mol.L―1
| 4×l0―6
| 6×l0―6
| 2×l0―5
| 4×l0―5
| 3×l0―5
| 2×l0―5
A.2 B.4 C.1 D.6
参考答案:B
本题解析:
试题分析:根据电荷守恒,c(H+)= [c(Cl-)+c(NO3-)+2c(SO42-)]-[c(K+)+c(Na+)+c(NH4+)]=l0―4mol.L―1,pH=4
考点:考查溶液中离子浓度的计算有关问题。
本题难度:一般
3、选择题 已知钾的氧化物有K2O2和KO2,在两种化合物组成的混合物中,钾与氧的质量比为13∶8,求混合物中K2O2与KO2的物质的量之比。
参考答案:混合物中K2O2与KO2的物质的量之比为1∶2。
本题解析:设混合物中K2O2与KO2的物质的量之比为x∶y,由K2O2、KO2组成可知:
n(K)∶n(O)=(2x+y)∶(2x+2y)
m(K)∶m(O)="39" g・mol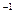 ×(2x+y)∶[16 g・mol ×(2x+y)∶[16 g・mol 本题难度:简单 本题难度:简单
4、填空题 (共7分)(1)0.5 mol H2SO4的质量是_______ g,含 个分子,含______mol氧原子,该硫酸所含氢元素的质量与  mol HCl中所含氢元素的质量相同。 mol HCl中所含氢元素的质量相同。
(2)在相同条件下,含有相同分子个数的SO2和SO3,其质量比为??????,物质的量比为??????,其中所含氧原子个数比为??????。
参考答案: 本题解析:略 本题解析:略
本题难度:一般
5、选择题 10.8 g X2O5中含有0.5molO,则X的相对原子质量为
A.21.6
B.28
C.14
D.31
参考答案:C
本题解析:略
本题难度:简单
|