微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2的物质的量之比为
A.3:4:1
B.3:3:2
C.6:7:3
D.6:9:0
参考答案:A
本题解析:
试题分析:可以设三种气体均为3mol,根据2Na2O2+2CO2==2Na2CO3+O2↑ ,体积变为原体积的8/9,利用差量法可知反应CO2为2mol,生成氧气1mol,这时混合气体中N2、O2、CO2的物质的量之比为3:4:1,A正确。
考点:考察元素及其化合物性质、化学反应的计算。
本题难度:一般
2、简答题 Ⅰ.下列实验方案不可行的是:______
A.用品红溶液鉴别CO2和SO2气体?????????B.用铜制容器盛放浓硝酸
C.用带玻璃塞的试剂瓶盛放NaOH溶液?????D.用NH3和H2O做喷泉实验
E.除去?N2?中少量的O2用灼热的铜网???????F.所有剩余的药品都不能放回原瓶
G.制Fe(OH)2时可将吸有NaOH溶液的滴管伸入到Fe?SO4溶液液面以下
Ⅱ.实验室制配0.5mol/L的NaOH溶液500mL.
(1)配制时,一般可分为以下几个步骤:①称量??②计算?③溶解?④摇匀⑤转移?⑥洗涤?⑦定容?⑧冷却.其正确的操作顺序为______.
(2)试分析下列操作对所配溶液的浓度有何影响.(填“偏高”、“偏低”或“无影响”)
①定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,对所配溶液浓度的影响______.
②某同学观察液面的情况如右图所示,则所配置的溶液的浓度______.
(3)取出其中50mL溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为______.
参考答案:Ⅰ.A.因SO2气体能使品红溶液褪色,而CO2气体不能使品红
本题解析:
本题难度:一般
3、选择题 设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,33.6L HF中含有氟原子的数目为1.5NA
B.常温常压下,9.2g二氧化氮和四氧化二氮的混合物含有氮原子的数目为0.2NA
C.50mL18.4mol・L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
D.0.1mol铁溶于足量氯水中,转移电子的总数为0.2NA
参考答案:
本题解析:
试题分析:A选项,标准状态下,HF为液态,故不能用气体公式计算,错误。B选项,N2O4=2(NO2),故9.2g二氧化氮和四氧化二氮的混合物相当于含有9.2gNO2或N2O4,故含有N原子数目为0.2NA,B正确。C选项,18.4mol・L-1浓硫酸,当反应一段时间后浓度变低,不再发生反应,故不能完全反应,生成SO2分子的数目小于0.46NA。C错误。D选项,由于氯水中含有次氯酸,具有强氧化性,能够将二价铁离子氧化为三价铁离子,故转移电子数为0.3NA。D错误。
本题难度:一般
4、选择题 用NA表示阿伏德罗常数,下列叙述正确的是(??)。
A.标准状况下,22.4 L H2O含有的分子数为1 NA
B.常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,1 NA个CO2分子占有的体积为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1NA
参考答案:B
本题解析:标准状况下,水不是气体,不能用于气体摩尔体积,A不正确。根据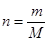 可知,1.06 g Na2CO3是0.01mol,含有0.02mol钠离子,B正确。1 NA个CO2分子是1mol,但状态不是在标准状况下,其体积不是22.4L,C不正确。D中溶液的体积不能确定,所以溶质的物质的量就不能确定,D不正确,答
可知,1.06 g Na2CO3是0.01mol,含有0.02mol钠离子,B正确。1 NA个CO2分子是1mol,但状态不是在标准状况下,其体积不是22.4L,C不正确。D中溶液的体积不能确定,所以溶质的物质的量就不能确定,D不正确,答
本题难度:一般
5、选择题 对于相同物质的量的SO2 和SO3 ,下列说法中正确的是 [???? ]
A.硫元素的质量比为5:4
B.分子数之比为1:1
C.原子总数之比为4:3
D.质量之比为5:4
参考答案:B
本题解析:
本题难度:简单