微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 将煤转化为水煤气的主要化学反应为:
C+H2O
高温
.
CO+H2
C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为:
C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol-1
H2(g)+1
2
O2(g)═H2O(g)△H=-242.0kJ?mol-1
CO(g)+1
2
O2(g)═CO2(g)△H=-283.0kJ?mol-1
请回答:
(1)根据以上数据,写出C(s)与水蒸气反应的热化学反应方程式:______.
(2)比较反应热数据可知,1molCO(g)和1molH2(g)完全燃烧放出的热量之和比1molC(s)完全燃烧放出的热量多.甲同学据此认为“煤转化为水煤气可以使煤燃烧放出更多的热量”;乙同学根据盖斯定律作出下列循环图(见图):
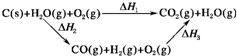
并据此认为“煤转化为水煤气再燃烧放出的热量与煤直接燃烧放出的热量相等”.
请分析:甲、乙两同学观点正确的是______(填“甲”或“乙”);判断的理由是______.
(3)将煤转化为水煤气作为燃料和煤直接燃烧相比有很多优点,请列举其中的两个优点______,
______.
(4)水煤气不仅是优良的气体燃料,也是重要的有机化工原料.
CO和H2在一定条件下可以合成:①甲醇、②甲醛、③甲酸、④乙酸.
试分析当CO和H2按1:1的体积比混合反应,合成上述______(填序号)物质时,可以满足“绿色化学”的要求,完全利用原料中的原子,实现零排放.
参考答案:(1)①C(石墨,s)+O2(g)═CO2(g)△H=-39
本题解析:
本题难度:一般
2、选择题 已知:2Zn(s)+O2(g)=2ZnO(s);△H=-701.0kJ?mol-1
2Hg(l)+O2(g)=2HgO(s);△H=-181.6kJ?mol-1
则反应Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为( ? ) A.+519.4kJ?mol-1
B.+259.7?kJ?mol-1
C.-259.7kJ?mol-1
D.-519.4kJ?mol-1
参考答案:C
本题解析:
本题难度:简单
3、填空题 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g)+2H2(g)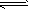 CH3OH(g) ΔH1 CH3OH(g) ΔH1
反应II:CO2(g)+3H2(g)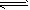 CH3OH(g) + H2O(g) ΔH2 CH3OH(g) + H2O(g) ΔH2
①下表所列数据是反应I在不同温度下的化学平衡常数(K)。
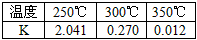
由表中数据判断ΔH1______0 (填“>”、“=”或“<”)。
②某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,5min后该反应达到平衡,测得c(CO)=0.2
mol/L,则用H2表示的该反应的反应速率为:________,此时的温度为________(从上表中选择)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) =2CO2(g) + 4H2O(g) ΔH =-1275.6 kJ/mol
② 2CO (g)+ O2(g) =2CO2(g) ΔH =-566.0 kJ/mol
③ H2O(g) =H2O(l) ΔH =-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:______________________
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。

①该电池正极的电极反应为__________________。
②用该电池电解200mL饱和食盐水(溶质足量),一段时间后,阴极得标况下气体2.24L,电解后溶液的pH为________(溶液体积变化忽略不计),要使电解后溶液复原,所加物质为___________(填名称)。
参考答案:(1)①<;②0.32mol·L-1·min-1;250℃
本题解析:
本题难度:一般
4、选择题 已知298K时下述反应:
①C(s)+1/2O2(g)=CO(g)△H1=-110.5kJ?mol-1
②CO(g)+1/2O2(g)=CO2(g)△H2=-283.0kJ?mol-1
③C(s)+CO2(g)=2CO(g)△H3,
则△H3等于( ? ) A.172.5kJ?mol-1
B.-172.5kJ?mol-1
C.393.5kJ?mol-1
D.-393.5kJ?mol-1
参考答案:A
本题解析:
本题难度:一般
5、填空题 常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为kJ/mol)下表是一些键能数据(kJ·mol-1)
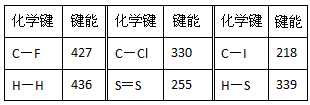
回答下列问题:
(1)由表中数据规律预测C-Br键的键能范围:_________<C-Br键能<_________
(2)热化学方程式2H2(g)+S2(g) ==2H2S(g) △H= QkJ·mol-1;则Q=___________
(3)已知下列热化学方程式:
O2(g) == O2+(g) +e- △H1= +1175.7 kJ·mol-1
PtF6(g) + e-== PtF6-(g) △H2= -771.1 kJ·mol-1
O2+PtF6-(s) == O2+(g) + PtF6-(g) △H3= +482.2 kJ·mol-1
则反应O2(g) +_________(g) = O2+PtF6-(s)的△H=_____________ kJ·mol-1。
参考答案:(1)218kJ·mol-1;330kJ·mol-1
本题解析:
本题难度:一般
|
网站客服QQ: 960335752 - 14613519 - 791315772
|
|