��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij������Һ��ֻ��N
H
+4
��Cl-��H+��OH-�������ӣ�����˵����ȷ���ǣ�������
A����Һ������Ũ�ȿ������㣺c(Cl-)��c(H+)��c(NH
+4
)��c(OH-)
B������Һ�����ɵ����ʵ���Ũ�ȡ������������Ͱ�ˮ��϶���
C������pH=3��������pH=11�İ�ˮ�������϶���
D����ͨ��������������Һ������Ũ�ȿ���Ϊ��c(NH
+4
)��c(Cl-)��c(H+)��c(OH-)
�ο��𰸣�A
���������
�����Ѷȣ���
2��ѡ���� ��֪ij��Һ�д���OH-��H+��NH4+��Cl-�������ӣ�����λͬѧ�ⶨ��Ũ�ȴ�С�Ĺ�ϵ���£����в����ܵ��ǣ� ? ��
A��c��Cl-����c��NH4+����c��H+����c��OH-��
B��c��Cl-����c��H+����c��NH4+����c��OH-��
C��c��Cl-����c��NH4+����c��OH-����c��H+��
D��c��OH-����c��H+����c��Cl-����c��NH4+��
�ο��𰸣�CD
���������
�����Ѷȣ�һ��
3�������
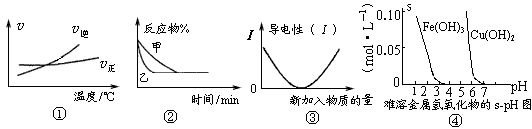
��һ�����£�CH3COOH��Һ�д��ڵ���ƽ�⣺CH3COOH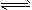 CH3COO-+H+ ��H>0
CH3COO-+H+ ��H>0
��1�����з����У�����ʹ0.10mol��L-1 CH3COOH��Һ��CH3COOH����̶��������____________��
a.��������0.10mol��L-1��ϡ���� b.����CH3COOHc.����ϡ����0.010mol��L-1 d.��������������
e.���������Ȼ��ƹ��� f.��������0.10mol��L-1��NaOH��Һ
��2��25��ʱ���õ���ƽ���ƽ��Ϊ1.75��10-5�����У�
��0.100.010mol��L-1 CH3COOH��Һ ��0.00100.010mol��L-1 CH3COOH��Һ ��c(H+)֮��Ϊ�٣���=______������ʾ�����м��㣬ƽ��ʱ��c(CH3COOH)������ʼŨ�ȴ��棬ˮ�������c(H+)��c(OH-)���Բ��ƣ���ͬ��
��3��25��ʱ����0.10mol��L-1 CH3COOH��Һ�м���һ��������CH3COONa��������Һ������䣩������Һ��c(CH3COO-)Ϊ1.0mol��L-1������Һ��c(H+)=________mol��L-1 ������������С�������λ��Ч���֣�����Һ�и�������Ũ�ȹ�ϵ��_________��
�ο��𰸣���1��bcf
��2��10��1
��3��c(CH
���������
�����Ѷȣ�һ��
4��ѡ���� ��ѧ�г���ͼ��ֱ�۵�������ѧ��Ӧ�Ľ��̻���������ͼ��������ȷ����
 [???? ]
[???? ]
A������ͼ�ٿ��жϿ��淴Ӧ��A2(g)+3B2(g)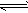 2AB3(g)���Ħ�H��0
2AB3(g)���Ħ�H��0
B��ͼ�ڱ�ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g)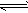 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ��
3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ��
C��ͼ�ۿɱ�ʾ������Һ��ͨ�백����������������Һ�����Եı仯
D������ͼ�ܣ�����ȥCuSO4��Һ�е�Fe3+�ɲ�������Һ�м�������CuO����pH��4����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5������� ij��ѧѧϰС��Ϊ�о�HA��HB��MOH������Ե����ǿ�����������ʵ������ʵ�飺��pH�T2����������ҺHA��HB��pH=12��MOH����Һ��1mL���ֱ��ˮϡ�͵�1000mL����pH�ı仯����Һ����Ĺ�ϵ��ͼ���������������ݣ���ش��������⣺
��1��HAΪ______�ᣬHBΪ______����ǿ����������
��2����c=9����ϡ�ͺ��������Һ�У���ˮ�����������Ũ�ȵĴ�С˳��Ϊ______�����ᡢ�ѧʽ��ʾ������ϡ�ͺ��HA��Һ��MOH��Һȡ�������ϣ���������Һ��c��A-����c��M+���Ĵ�С��ϵΪ______��������ڡ�����С�ڡ����ڡ���
��3����b+c=14����MQHΪ______��ǿ��������������ϡ�ͺ��HB��Һ��MOH��Һȡ�������ϣ����úܺ���Һ��pH______7������ڡ�����С�ڡ����ڡ���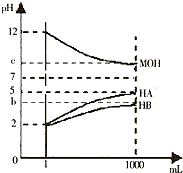
�ο��𰸣���1����ͼ��֪��pH�T2����������ҺHA��HB��1mL���ֱ�
���������
�����Ѷȣ�һ��
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772