微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (15分)
A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,甲、乙则是两种单质,以上单质和化合物之间在如图1所示的反应关系(反应物和生成物均无省略)。

请回答下列问题:
(1)图1所示转化过程中包含的反应类型有??????????(填字母)。
a.置换反应??? b.复分解反应????? c.分解反应??? d.化合反应
(2)图1中反应①的化学方程式是????????????????????????????????。(3分)
(3)图1中反应③在一定条件下为可逆反应,反应的能量变化如图2所示,当该反应处于平衡状态时,下列措施中有利于提高C的平衡转化率的是?????????????(填字母)。
A.升高温度??? B.降低温度??????? C.增大压强
D.减小压强??????????????????????? E.加入催化剂????? F.增加C的量
(4)若将l.00 mol甲和2.00 mol C混合充入容积为2 L的密闭容器中,3分钟后反应达到平衡。平衡后混合气体总物质的量为2.55mol,用甲表示的化学反应速率为
?????????mol?L-1?min-1。
(5)容积均为2 L的四个密闭容器中均进行着(4)中的反应,某温度下,各物质物质的量(mol)及正逆反应速率关系如下表所示:
容器编号
| n(甲)
| n(C)
| n (D)
| v正与v逆的关系
|
Ⅰ
| 0.20
| 0.10
| 0.20
| v正=v逆
|
Ⅱ
| 0.20
| 0.40
| 1.00
| ②?
|
Ⅲ
| 0.60
| 1.20
| 0.80
| ③?
①若方程式系数为最简整数比,则该温度下的平衡常数K=??????????????????????
填写表中空格:?②???????????????③???????????????
2、选择题 下列对熵的理解不正确的是
A.同种物质气态时熵值最大,固态时熵值最小
B.体系越有序,熵值越小;越混乱,熵值越大
C.与外界隔离的体系,自发过程将导致体系的熵减小
D.25 ℃、1.01×105 Pa时,2N2O5(g)====4NO2(g)+O2(g)是熵增的反应
3、选择题 在一恒温、恒容的密闭反应器中发生如下反应:C(s)+H2O?CO(g)+H2(g),为了判定该可逆反应是否达到平衡,没有参考价值的物理量是( )
A.反应器内气体的总压强
B.反应器内气体的总的物质的量
C.反应器内固体的总质量
D.反应器内物质的总质量
4、填空题 某温度下,将2mol A和2.8 mol B充入体积为2 L的恒容密闭容器中,发生如下反应:
aA(g)+B(g) 2C(g)+ D(s) ,5 min后达到平衡。平衡时A为1.6mol,放出的热量为Q。在t0时刻,若从平衡体系中分离出四分之一的混合气体,新平衡体系中c(A)为0.6mol/L。 2C(g)+ D(s) ,5 min后达到平衡。平衡时A为1.6mol,放出的热量为Q。在t0时刻,若从平衡体系中分离出四分之一的混合气体,新平衡体系中c(A)为0.6mol/L。
(1) 5 min内用B表示该反应的化学反应速率为?????????????????。
(2)该温度下,此可逆反应的逆反应的平衡常数为??????????。
(3)a的值为??????????。
(4)下列说法一定能说明上述反应已达到平衡状态的是??????????。
①单位时间里每生成1molB的同时消耗了2mol的C?????????②D的物质的量不再变化
③混合气体的密度不再变化?????????④混合气体的平均相对分子质量不再变化
⑤体系的压强不再变化
(5)该温度下,某同学设计了以下实验,请在空格中填入热量(含Q的表达式表示)
起始
n(A)/mol
| 起始
n(B)/mol
| 起始
n(C)/mol
| 起始
n(D)/mol
| 达到平衡时放出(或吸收)的热量
| 0
| 1.6
| 8
| 足量
| ????
?
5、填空题 在某一容积为5 L的密闭容器内,加入 0.3 mol的CO和0.3 mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g)??ΔH>0,反应中CO2的浓度随时间变化情况如图: CO2(g)+H2(g)??ΔH>0,反应中CO2的浓度随时间变化情况如图:
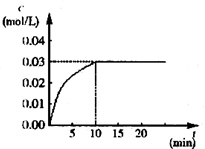
(1)根据图上数据,反应开始至达到平衡时,CO的化学反应速率为v(CO)=??????????mol/(L・min)-1,该温度下的平衡常数K=????????????。
(2)在体积不变的条件下,改变下列条件重新达到平衡时能使平衡常数K增大的有????????(填字母)
A升高温度;B降低温度;C增大压强;D减小压强;E加入催化剂;G移出一氧化碳气体
(3)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.2 mol的CO2和0.2 mol的H2,在相同的条件下,反应达平衡时,c(CO)=?????????????????mol/L。
(4)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol 的水蒸气,重新达到平衡后,CO的转化率????????(填“升高”、“降低”还是“不变”),CO2的质量分数????????(填“升高”、“降低”还是“不变”)。
(5)在催化剂存在和800℃的条件下,在某一时刻测得c(CO)=c(H2O)=0.09mol/L,c(CO2)=c(H2)=0.13mol/L,则此反应是否处于平衡状态????????(填“是”或“否”),若没有处于平衡状态则该反应向????????移动。(填“正方向”或“逆方向”)
|
|