微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 A2+B2===2AB的反应历程可以看作如下(△H表示该过程的能量变化):
Ⅰ.A2==="A" +A △H 1 Ⅱ.B2==="B" +B △H 2 Ⅲ.A+B===AB △H 3
则下列说法中正确的是( )
A.当△H3+(△H1+△H2) >0时,该反应是吸热反应;
B.当 2△H3+(△H1+△H2) > 0时,该反应是放热反应;
C.当 2△H3+(△H1+△H2 ) <0时,该反应是放热反应;
D.当1/2△H3+(△H1+△H2)<0时,该反应是吸热反应;
参考答案:C
本题解析:
试题分析:根据盖斯定律可知,I+Ⅱ+Ⅲ×2即得到反应A2+B2===2AB,所以该反应的反应热是△H= 2△H3+(△H1+△H2 )。因此选项C正确,答案选C。
考点:考查反应热的计算和判断
点评:在根据多个热化学方程式计算有关的反应热时,盖斯定律是最重要的定律,需要熟练掌握并能灵活运用。
本题难度:一般
2、填空题 (8分)卤族元素的单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示卤族中某一元素的单质, E为相同物质的量的单质与H2反应过程中的能量变化(
E为相同物质的量的单质与H2反应过程中的能量变化( E越大,表明反应越容易发生)。
E越大,表明反应越容易发生)。
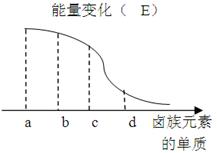
请回答下列问题:
d为_____(写化学式) ,红热的铜丝在b单质中燃烧的现象为 .
b与H2反应的条件为______________ .
(2)由该能量变化示意图可得出的结论是同一主族,自上而下,元素的非金属性依次 .
参考答案:(1)I2;剧烈燃烧,产生棕黄色的烟 (2)点燃(
本题解析:(1)非金属性越强,越容易和氢气化合,放出的热量越多,所以a、b、c、d分别是F、Cl、Br、I。铜在氯气中燃烧的现象是剧烈燃烧产生棕黄色的烟。氯气和氢气通过点燃或光照均可以反应,生成氯化氢。
(2)由该能量变化示意图可知,同一主族,自上而下,元素的非金属性依次减弱。
本题难度:一般
3、选择题 下列物质中,既有离子键又有共价键的是
A.Ca(NO3)2
B.KOH
C.H2O
D.NH4F
参考答案:ABD
本题解析:钙离子与硝酸根间形成离子键,硝酸根内氮、氧原子间形成共价键;
钾离子与氢氧根间形成离子键,氢氧根内氢、氧原子间形成共价键;
H2O中仅存在氢、氧原子间的共价键;
铵根、氟离子间形成离子键,铵根内氮、氢原子间形成共价键;
本题难度:一般
4、选择题 将4 mol A 气体和2 mol B 气体在2 L的容器中混合并在一定条件下发生反应2A(g)+B(g) 2C(g)。若经2 s后达到平衡,测得C 的浓度为0.6 mol・L-1。则下列说法正确的是(???)
2C(g)。若经2 s后达到平衡,测得C 的浓度为0.6 mol・L-1。则下列说法正确的是(???)
A.用物质A 表示的反应的平均速率为0.6 mol・L-1・s-1
B.用物质B 表示的反应的平均速率为0.3 mol・L-1・s-1
C.2 s 时物质A 的转化率为70%
D.2 s 时物质B 的浓度为0.7 mol・L-1
参考答案:D
本题解析:C的浓度为0.6 mol・L-1,用物质C 表示的反应的平均速率为0.3 mol・L-1・s-1,用物质A表示的反应的平均速率为0.3 mol・L-1・s-1,所以A项错误;用物质B 表示的反应的平均速率为0.15 mol・L-1・s-1,所以B错误;2 s 时物质A的转化率应为30%,所以C项错误。本题要注意的是:容器的体积是2 L,时间是2 s。
本题难度:简单
5、选择题 对于反应A2+3B2=2C+D,化学反应速率最快的是
A.V(B2)=0.8mol/(L・s)
B.V(D)=0. 6mol/(L・s)
C.V(C)=0.6mol/(L・s)
D.V(A2)=0.8mol/(L・min)
参考答案:B
本题解析:在同一化学反应方程式中,不同的物质表示的反应速率可能不同,但是意义完全相同,均表示该反应的反应速率。解此题只需将各选项中的物质转化为相同的物质的反应速率即可判断其反应速率的大小。
以V(B2)为标准;B选项,V(B2)="3" V(D)=" 1." 8mol/(L・s);
C选项,V(B2)=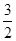 ?V(C)="0.9" mol/(L・s)????;
?V(C)="0.9" mol/(L・s)????;
D选项,V(B2)="3" V(A2)=2.4 mol/(L・min) ="0.04" mol/(L・s)
所以最快的为B选项。
本题难度:一般