微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将一严重锈蚀而部分变成铜绿[Cu2(OH)2CO3 ]的铜块研磨成粉末,在空气中充分灼烧到质量不再变化为止,固体质量的变化情况不可能是
A.不变
B.增重10%
C.增重30%
D.减轻20%
参考答案:C
本题解析:采用极值法来考虑
Cu2(OH)2CO3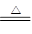 2CuO+H2O↑+CO2↑
2CuO+H2O↑+CO2↑
222g??????????? 160g
固体Cu2(OH)2CO3转化为CuO,固体质量减少:62/222=27.9%
2Cu+O2=2CuO
64g?????? 80g
固体由铜转化为氧化铜,固体质量增
本题难度:简单
2、实验题 (15分)实验室以废铜屑为原料制取碱式碳酸铜【Cu2(OH)2CO3】的步骤如下:
步骤一:废铜屑制硝酸铜
如图,
用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。
步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠溶液和硝酸铜溶液,水浴加热至70℃左右,用0.4?mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。?
步骤三:碱式碳酸铜的组成测定
碱式碳酸铜可表示为:xCuCO3 ・yCu (OH)2 ・zH2O,可采用氢气还原法来确定,其反应原理为:
xCuCO3 ・yCu (OH)2 ・zH2O +? H2→ Cu +? CO2 ?+? H2O(未配平)
完成下列填空:
(1)步骤一中,反应开始时,瓶内的现象是???????????????????????????????????????,
用该装置制取硝酸铜,好处是??????????????????????????????????????????????????。
(2)步骤二中,水浴加热所需仪器有????????????????、??????????????????(加热、夹持仪器、石棉网除外);洗涤的目的是?????????????????????????????????????????。
(3) 步骤三中,①以字x、y、z母为系数,配平氢气还原法的化学方程式:
??????xCuCO3 ・yCu (OH)2 ・zH2O+ ??????H2→?????Cu+ ?????CO2+ ?????H2O
②称取24.0g某碱式碳酸铜样品,充分反应后得到12.8 g残留物,生成4.4g二氧化碳和7.2g水。该样品中结晶水质量为????????g,化学式为??????????????????。
参考答案:(1)气体变为红棕色,锥形瓶中溶液变蓝色;?减少氮氧化合物对
本题解析:
试题分析:(1)在实验步骤一中,反应开始时,会看到在Cu 溶解,锥形瓶中溶液变蓝色,气体变为红棕色。由于该实验装置是密闭的,产生的大气污染物NO2、NO会被NaOH溶液吸收,减少氮氧化合物对环境的污染;(2)在操作步骤二中,水浴加热所需仪器有烧杯、温度计;洗涤的目的是除去产品表面吸附的杂质硝酸钠;(3) ①根据元素守恒、电子守恒可得方程式为xCuCO3 ・yCu (OH)2 ・zH2O+(x+y)H2→(x+y)Cu+x CO2↑+(x+2y+z)H2O。②n(Cu)=" 12.8" g÷64g/
本题难度:一般
3、填空题 (6分)已知A为生活中最常见金属,有以下物质相互转化

试回答:(1)写出B的化学式??????????,D的化学式???????????。
(2)写出由E转变成F的化学方程式??????????????????????????????。
(3)向G溶液加入A的有关离子反应方程式????????????????????????????。
参考答案:(1)B:FeCl2,D:KCl。(2)? 4Fe(OH)2
本题解析:
试题分析:A为生活中最常见金属即为本题的突破口,是铁,铁一般与酸反应产生氢气和亚铁离子;又因为D溶液与硝酸银反应生成白色沉淀,说明含有氯离子,白色沉淀在空气中迅速转化为红褐色沉淀,说明E为氢氧化亚铁,F为氢氧化铁,G为氯化铁,B为氯化亚铁,D为氯化钾,H为氯化银。(1)B的化学式为FeCl2,D的化学式为KCl。(2)E到F即氢氧化亚铁与氧气和水反应生成氢氧化铁: 4Fe(OH)2+O2+2H2O=4Fe(OH)3。(3)氯化铁与铁生成的是氯化亚铁:Fe+2Fe3+=3Fe2+。
点评:抓住
本题难度:一般
4、选择题 为了预防缺铁性贫血,人体必须保证足够的铁的摄入。这里的“铁”是指(???)
A.铁单质
B.铁元素
C.氢氧化铁
D.氧化铁
参考答案:B
本题解析:人体血红蛋白中含Fe2+,故指铁元素。
本题难度:简单
5、填空题 古代的药金外观与黄金相似,常被误认为是金子。其冶炼的方法是:将炉甘石(碳酸锌)、赤铜(Cu2O)、和过量的木炭混合加热到800℃,即得金光闪闪的“药金”。请回答下列问题:
(1)“药金”的主要成分是???????????????;
(2)有关化学反应方程式是??????????????????????????????????????????????;
(3)区别“药金”与黄金的化学方法是????????????????????????????????????。
参考答案:(1)铜锌合金?
 本题解析:根据题意结合所学的知识可知,800 ℃的高温下ZnCO3肯定会分解产生CO2和ZnO,而木炭则能在高温下将ZnO和Cu2O中的金属分别还原出来,被还原出来的两种金属便会熔合而成合金。运用元素守恒原理很容易判断知整个过程中不可能生成新元素金,即所得到的黄色物质中不可能有金。
本题解析:根据题意结合所学的知识可知,800 ℃的高温下ZnCO3肯定会分解产生CO2和ZnO,而木炭则能在高温下将ZnO和Cu2O中的金属分别还原出来,被还原出来的两种金属便会熔合而成合金。运用元素守恒原理很容易判断知整个过程中不可能生成新元素金,即所得到的黄色物质中不可能有金。
本题难度:简单