��
?
������γɵ�Һ�廯�����dz������ܼ������Ԫ�������ڱ��е�λ����??????����Ԫ�ص�������ĵ���ʽ��????????��������γɵĻ������д��ڵĻ�ѧ����??????����ڡ��ߡ�������Ԫ������������Ӧ��ˮ��������������ǿ��˳����??????????(�û�ѧʽ��ʾ)���ߡ�������Ԫ���γɵ������Ӱ뾶��С˳����?????????(�����ӷ�����)��
��2�����ס����������������Ϊ����������Ԫ������ɵĵ��ʻ���Ҽס��ҡ���Ϊ��ɫ���壬��Ϊ����ɫ���塣������ͼ��ʾת����ϵ�Ʋ⣺
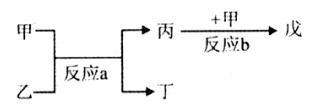
��д����Ӧa�Ļ�ѧ����ʽ��?????????????????????????��
��д�����붡��Ӧ�Ļ�ѧ����ʽ��????????????????????��
��3������ͼ��A��B��C��D��E�ֱ�������10��Ԫ����ɵĵ��ʻ��
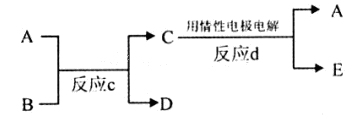
������Ӧc����A�����ص����������B��ˮ��Һ������A�Ǻ�ɫ�������ʣ�E�Ǿ��л���ɫ�����塣��Ӧd�������ĵ缫��ӦʽΪ��???????????��
������Ӧc���ڸ����½��еġ�����B�ǰ���ɫ���壬������C��һ�����Ի������Ӧc�Ļ�ѧ����ʽΪ????????????????????��
�ο��𰸣���1���������ڵڢ�A����2�֣� ��������� ���������
�����������1���ڵ�ԭ��������������1���ɢ������ڱ��е�λ�ÿ�֪���ڴ��ڵڶ����ڣ��ߢദ�ڵ������ڣ�������γɵ�Һ�廯�����dz�������Ҫ�ܼ����û�����ΪSC2��CCl4���ɢڢߢ��λ�ÿ�֪����Ϊ̼����Ϊ��Ϊ�ȣ�������γɵ�Һ�廯����ΪCCl4��Sԭ��ԭ����3�����Ӳ㣬����������Ϊ6���������ڱ��е������ڵڢ�A�壻������̼������̼ԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ�����ʽΪ �����Ѷȣ�һ�� �����Ѷȣ�һ��
2������� ��һ�������£�ijЩ��ѧ��Ӧ��������ͼ��ܱ�ʾ������Ҫ��ش��������⣺
��1����A��C��D��Ϊ�������ʣ���A�Ļ��ϼ۽���C��D֮�䣬D����Ư���ԣ�д���÷�Ӧ�����ӷ���ʽ______��
��2����ͨ�����ķ�����û���ɫ����C����÷�Ӧ�����ӷ���ʽΪ______
��3����C��D��Ϊ�����Ҿ���ʹ����ʯ��ˮ����ǣ�д������������ͼҪ��Ļ�ѧ����ʽ______
��4����AΪ��ɫ�������ʣ�BΪ�ڶ�����ij��Ԫ�ص�����������ˮ�����ϡ��Һ��
д������������ͼ��ϵ�����ӷ���ʽ______��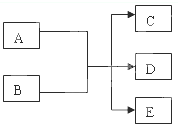
�ο��𰸣���1����A��C��D��Ϊ�������ʣ���A�Ļ��ϼ۽���C��D֮�䣬
���������
�����Ѷȣ���
3������� ��8�֣���ѧ������ij��Ӧ�Ļ�ѧ����ʽΪA+B��C+D+H2O��δ��ƽ����Ӧ������ȥ������ش������й����⣺
��1����A������B��ϡ���ᣨ����������A������C��Һ�С���A��C��Ӧ�����ӷ���ʽΪ_________________________________________________________________��
��2����C��D��Ϊ���壬�Ҷ���ʹ����ʯ��ˮ����ǣ���������Ӧ �Ļ�ѧ����ʽΪ___________________________________________________________________________�� �Ļ�ѧ����ʽΪ___________________________________________________________________________��
��3����C����ɫ�̼�����ζ�����壬��ˮ��Һ�������ԡ�C�ܷ�����������Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ____________________________________________________��
��4����DΪ�ȼҵ����Ҫԭ�ϣ�C���������ЧӦ����Ҫ����֮һ����������Ӧ�Ļ�ѧ����ʽΪ_____________________________________________________��
�ο��𰸣���1��2Fe3++Fe= ����������� �����������
�����Ѷȣ�һ��
4������� ��14�֣�A��J����ѧ��ѧ�г��������ʣ�����֮���ת����ϵ���¿�ͼ��ʾ�����ֲ�������ȥ������֪A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ������

��ش��������⣺
(1)A�Ļ�ѧʽΪ??????????��
(2)H��I��Һ��Ϻ�����Ӧ�����ӷ���ʽ��????????????????��
G��J�Ļ�ѧ����ʽΪ??????????????????????????��
(3)D����ǡ������һ������ϡ������ú��ʵĻ�ѧ�����ʾ������Һ������ԭ��?????????????��
(4) ʵ��֤�������ᷢ��������ԭ��Ӧʱ������Խϡ��Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡһ������C��E�Ͻ���һ�����ĺ�ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ�У���μ���һ��Ũ�ȵ�����������Һ�������������Ƶ����ʵ���������ij��������ʵ�����mol���Ĺ�ϵ����ͼ��ʾ���Իش��������⣺
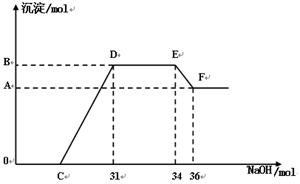
��ͼ��OC��û�г������ɣ��˽η��������ӷ���ʽΪ��_______________________________��
����DE��û�г��������ʵ���û�б仯����˽η�����Ӧ�����ӷ���ʽΪ��_________________________________��
��B���Ӧ�ij�����Ϊ________________ mol,C���Ӧ�ĺ�����Ϊ___________mol��
�ο��𰸣���1��Al2O3��2�֣�
��2��3AlO2����Al3��
�������������������ͼ�⣬�ؼ�����ͻ�Ƶ㡣A��һ�ָ��۵����ʣ�J��һ�ֺ��ɫ����������A����������J��������������D����������C������B��������E������F���Ȼ�������G��������������H��ƫ�����ƣ�I���Ȼ�����
��1���������Ȼ�ѧʽ��Al2O3��
��2��ƫ�����ƺ��Ȼ���ˮ����ٽ�������������������Ӧ�ķ���ʽ��3AlO2����Al3����6H2O=4Al(OH)3�����������������ȶ������ױ�����������������������ʽ��4Fe(OH)2+2H2O+O2�T4Fe(OH)3 ��
��3���������������������Ȼ�
�����Ѷȣ�һ��
5������� ��֪A��H����ѧ��ѧ�еij������ʣ�A��C��G�ǽ�����E��F�������B����ˮ����ɫ��Һ������������ͼ��ʾ�Ĺ�ϵ����Ӧ�����ɵ�ˮ����ȥ����
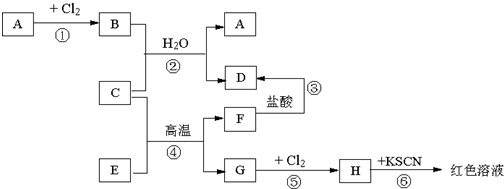
�Իش��������⣮
��1���ƶ���д���ʻ�ѧʽ��A��______��D��______��H��______��
��2��F�������______��ѡ��������������������������������������
��3����Ӧ�ܵĻ�ѧ����ʽΪ______��
�ο��𰸣�A��C��G�ǽ�����G��������Ӧ����H��H��KSCN��Ӧ����Һ
���������
�����Ѷȣ�һ��
|