微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对某溶液有如下操作:
①向该溶液中加入过量的盐酸生成白色沉淀;
②过滤后向滤液中加入过量的氨水(使溶液呈碱性),又有白色沉淀生成;
③再过滤后向滤液中加入碳酸钠溶液,又生成白色沉淀.
原溶液中含有的离子可能是
A.Ag+、Cu2+、Ba2+
B.Ag+、Ba2+、Al3+
C.Ag+、Fe3+、Ca2+
D.Al3+、Mg2+、K+
参考答案:B
本题解析:分析:①加入过量盐酸,生成的白色沉淀是氯化银;
②加入氨水,产生白色沉淀可能是氢氧化铝、氢氧化镁等;
③白色沉淀可能是碳酸钙、碳酸钡等;
根据以上分析进行判断.
解答:①向该溶液中加入过量的盐酸生成白色沉淀,白色沉淀为氯化银,溶液中一定存在银离子;
②过滤后向滤液中加入过量的氨水(使溶液呈碱性),又有白色沉淀生成,白色沉淀为强氧化物沉淀,可能是氢氧化镁、氢氧化铝等;
③再过滤后向滤液中加入碳酸钠溶液,又生成白色沉淀,白色沉淀为碳酸盐沉淀,可能是碳酸钡、碳酸钙等;
A、不可能有铜离子,氢氧化铜是蓝色沉淀,故A错误;
B、三种离子符合以上分析,故B正确;
C、氢氧化铁是红褐色沉淀,所以不可能存在铁离子,故C错误;
D、①中加入过量盐酸,Al3+、Mg2+、K+中没有能够生成沉淀的离子,故D错误;
故选B.
点评:本题考查了常见离子的检验,注重了基础知识的考查,本题难度不大.
本题难度:困难
2、填空题 为了防止或减少机动车尾气和燃煤产生的烟气对空气的污染,人们采取了很多措施。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g)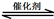 2CO2(g)+ N2(g) △H<0,
2CO2(g)+ N2(g) △H<0,
若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量、质量分数)
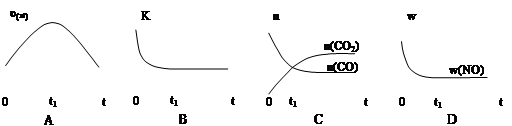
(2)机动车尾气和煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染。已知:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol ①
2NO2(g)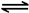 N2O4(g) ΔH=-56.9 kJ/mol ②
N2O4(g) ΔH=-56.9 kJ/mol ②
H2O(g) = H2O(l) ΔH=-44.0 kJ/mol ③
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
(3)用NH3催化还原NOX也可以消除氮氧化物的污染。如图,采用NH3作还原剂,烟气以一定的流速通过催化剂,通过测量逸出气体中氮氧化物含量,从而可确定烟气脱氮率,反应原理为:NO(g) +NO2(g)+2NH3(g)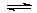 2N2(g) + 3H2O(g)。
2N2(g) + 3H2O(g)。
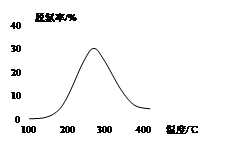
①该反应的△H 0(填“>”、“=”或 “<”)。
②对于气体反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作KP),
则上述反应的KP= 。
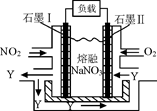
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图,石墨I为电池的 极。 该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为 。
(5)硝酸工业尾气中氮氧化物(NO和NO2)可用尿素〔CO(NH2)2〕溶液除去。反应生成对大气无污染的气体。1 mol尿素能吸收工业尾气中氮氧化物(假设NO、NO2体积比为1
参考答案:
本题解析:
本题难度:一般
3、选择题 实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学用实验比较法设计了如下实验方案,将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
A.t1 < t2 < t3 < t4
B.V4=V5=10
C.V6=7.5
D.V1<V2<V3<20
参考答案:C
本题解析:因为该实验是来研究硫酸铜的量对氢气生成速率的影响,因此要保证锌和硫酸完全一致,即V1、V2、V3均是20ml。要保证实验中硫酸的浓度相等,由实验丁可知所加饱和硫酸铜溶液的体积和水的体积之和一定是10ml,所以V6=7.5ml,V5=10ml,V4=2ml。因为实验甲中不能构成原电池,反应慢,用时多,所以正确的答案是C。
本题难度:一般
4、选择题 下列式子正确的是(??? )
A.H×
B.Na×+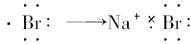
C.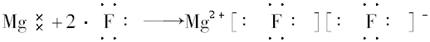
D.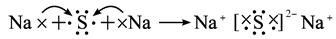
参考答案:D
本题解析:在元素符号周围用・或×来表示元素原子最外层电子的数目,这种式子叫电子式。
从题意看,是检查用电子式表示离子或分子形成的过程。检查时注意:
(1)阴、阳离子是否已标明电荷数;
(2)阴离子必须加括号,表示得到电子;
(3)阴或阳离子相同时不能合并写。
A不正确,因为H不是金属原子,故与氯化合后不是离子化合物,不能用“[?]”表示;B项错在阴离子未用方括号括起,未标出电荷;C项错在相同的阴离子排在一起。D项正确。
本题难度:一般
5、选择题 下列说法正确的是
A.甲烷的标准燃烧热为-890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)===CO2(g)+2H2O(g)△H=" -890.3" kJ/mol
B.500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:
C.已知:2CO(g)+O2(g) ===2CO2(g)ΔH=" -566" kJ/mol,下图可表示由CO生成CO2的反应过程和能量关系
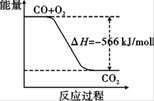
D.已知:1mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1mol F-F 、S-F键需吸收的能量分别为160 kJ、330 kJ。已知1个 SF6(g)分子中含有6条S-F键。则:S(s)+3F2(g) ===SF6(g) △H=-1220 kJ/mol
参考答案:D
本题解析:
试题分析:A.甲烷的标准燃烧热生成的产物必须是液态水,故错误;B、0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,因反应为可逆反应,则1molN2和3molH2置于密闭的容器中充分反应生成NH3(g),放热不是38.6kJ,则热化学反应方程式中的反应热数值错误,故错误;C.已知:2CO(g)+O2(g) ===2CO2(g)??ΔH=" -566" kJ/mol,右图可表示由1molCO生成CO2的反应过程和能量关系,而该方程式表示的是2mol参加的
本题难度:一般