��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �����͵������ﶼ����Ҫ�Ļ���ԭ�ϣ�������������Ի��������Ⱦ��
������֪��2KMnO4+16HCl��Ũ��= 2KCl+2MnCl2+5Cl2��+ 8 H2O����ʵ���ҿ��ö������̹���������ع����Ũ���ᷴӦ��ȡ�������ɹ�ѡ�õķ���װ������ͼ��
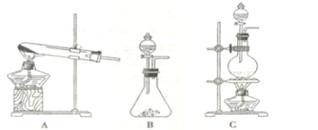
��1�����ø�����ع����Ũ���ᷴӦ��ȡ����������װ����??????��(ѡ��A��B��C)
��2��д���ö������̹����Ũ���ᷴӦ��ȡ�����Ļ�ѧ����ʽ��???????????????????��
��3������NaOH��Һ����������ֹ��Ⱦ��д���÷�Ӧ�����ӷ���ʽ????????????????��
������֪��NO2+NO+2NaOH=2NaNO2+H2O����������������Һ�������շ����еĵ������
��1���ڸ÷�Ӧ�У���������????????��???
��2������β���к���һ��������һ����̼�������������еĴ�ת����ת��Ϊ�Դ�������Ⱦ�����ʡ�д���÷�Ӧ�Ļ�ѧ����ʽ��?????????????????????????????????��
�ο��𰸣�����1��B?��2�� 4HCl(Ũ)+MnO2![]()
���������
�������������1���ø�����ع����Ũ���ᷴӦ��ȡ���������������Ӧ�������ǹ����Һ�岻���������壬ѡ����װ��B����2������������Ũ�����ڼ��������·�Ӧ���ɶ��Ȼ��̡�������ˮ����Ӧ����ʽΪ��4HCl(Ũ)+MnO2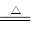 MnCl2+Cl2��+2H2O��3������������������Һ��Ӧ�����Ȼ��ơ�����������ˮ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��
MnCl2+Cl2��+2H2O��3������������������Һ��Ӧ�����Ȼ��ơ�����������ˮ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO-+H2O��
����1����ӦNO2+NO+2NaOH�T2NaNO2+H2O�У�NO2��NԪ�ػ��ϼ���+4�۽���ΪNaNO2�е�+3�ۣ�NO2������������2��һ��������һ����̼�����������еĴ�ת����ת��Ϊ�Դ�������Ⱦ�����ʣ�Ӧ���ɵ�����������̼����Ӧ����ʽΪ��2NO+2CO N2+2CO2��
N2+2CO2��
�����Ѷȣ�һ��
2��ʵ���� ��ͼ��ʾװ�ÿ�������ȡFe(OH)2�۲�Fe(OH)2�ڿ����б�����ʱ����ɫ�仯��ʵ��ʱ����ʹ����м��6 mol/L H2SO4��Һ��NaOH��Һ����д���пհף�
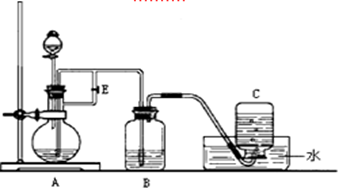
��1��B��ʢ��һ������??????????????��A��ӦԤ�ȼ�����Լ���?????????��A�з�Ӧ�Ļ�ѧ����ʽΪ????????????????????????????????????????��
��2��ʵ�鿪ʼʱӦ�Ƚ�����E???????������رա�����Ŀ����??????????????????????????????????��
��3��A��Ӧһ��ʱ�����E???????������رա�����Ŀ����???????
????????????????????????????????????��
��4��ʵ���������ȥװ��B�е���Ƥ����ʹ�������룬Fe(OH)2������������Ӧ������ת����0.04mol���ӣ���μӷ�Ӧ�����������Ϊ?????????L����״������
�ο��𰸣���1��NaOH��Һ?��м?? Fe+H2SO4===FeSO
�����������ȡFe(OH)2�Ĺؼ��Ƿ�ֹ������������Ԥ���ų�װ���еĿ������������װ�ü�ҩƷ����ȡFe(OH)2��FeSO4��2NaOH=Fe(OH)2����Na2SO4����ͨ����ӦFe��H2SO4=FeSO4=H2���������������ų�װ���еĿ�����
��1������װ�������Ժ���A��ƿ�з�����м����Һ©����װ��ϡ���ᣬB��ʢ��NaOH��Һ
��2��ʵ�鿪ʼʱӦ�Ƚ�����E����Һ©���Ļ��������������������ɵ���������װ�ú���Һ�еĿ���
��3��A��Ӧһ��ʱ�����E�رգ���������������ʹ��ƿ��ѹǿ����A��FeSO4��Һѹ��B�з�Ӧ�������е�NaOH��Һ��Ӧ���ɰ�ɫFe(OH)2������
��4��ʵ���������ȥװ��B�е���Ƥ����ʹ�������룬Fe(OH)2��������������ɫ�ɰ�Ѹ���û�Ϊ����ɫ������ת��Ϊ���ɫ�����ʵ��
��4Fe(OH)2��O2��2H2O=4Fe(OH)3��֪����Ӧ����4�����ӵ�ת�ƣ�����Ӧ������ת����0.04mol���ӣ���μӷ�Ӧ������Ϊ0.01mol����״�������Ϊ0.224L
�����Ѷȣ���
3��ѡ���� ���������У���������ˮ���ռ�����
A��NO2
B��NO
C��O2
D��H2
�ο��𰸣�A
���������
�������������������ܽ��ԡ��Ƿ��������Ӧ��������ܶ���ȷ��������ռ�����������ˮ����ˮ��Ӧ�����岻������ˮ���ռ�����������Ӧ�����岻�����ſ������ռ���A��NO2������ˮ����ˮ��Ӧ����������ˮ���ռ�����ȷ��B��NO������ˮ�Һ�ˮ����Ӧ����������ˮ���ռ�������C������������ˮ�Һ�ˮ����Ӧ����������ˮ���ռ������� D������������ˮ�Һ�ˮ����Ӧ����������ˮ���ռ�������
�����Ѷȣ�һ��
4��ʵ���� ��17�֣���ѧ������3.0 mol��L-1ϡ������̽����ʵ�飬����ʱʵ����ֻ��18.4 mol��L-1Ũ���ᡣ����Ϊ������100 mL 3.0 mol��L-1ϡ���ᡣ
��1)�������ƹ������£�
�ټ�������Ũ����������????????(ȷ��С�����һλ)����ȡŨ�������õ���Ͳ�Ĺ����???����������ѡ��A.10 mL��B.25 mL��C.50 mL��D.100 mL����
��ϡ�͡��������������??????????????????????????????????????????��
�۴��ϲ��õ���ϡ��Һ�����ȴ����������������ע��?????????��������ˮϴ���ձ��ڱںͲ�����2-3�Σ�ϴ��ҺҲע�����С�����ҡ������ƿ��ʹ��Һ��Ͼ��ȡ�
�ܽ�����ˮע������ƿ����Һ��������ƿ�̶���1-2cm������?????��ˮ��Һ����̶������С��Ǻ�ƿ�����������µߵ���ҡ�ȡ�
�ݽ���õ���Һת�Ƶ��Լ�ƿ�У�����ͬѧʹ�á�
��2����������Һ�����У������������ʱ��ʵ��Ũ�Ȼ�����������ƫ�ߡ�ƫ�ͻ�Ӱ�죩
A.���õ�Ũ���᳤ʱ��������ܷⲻ�õ�������????????????
B.����ƿ������ˮϴ�Ӻ������������ˮ????????????
C.���ù����ձ���������δϴ��?????????????
D.����ʱ���ӿ̶���?????????????
�ο��𰸣�16.3mL? B��25mL��1�֣�����ÿ��2�֣�??��װ��
���������
�����������1��1����Ũ��������ΪV��18.4mol/L��V=0.1L��3.0mol/L��V=0.0163L=16.3mL��ѡȡ��Ͳ���ݻ�Ӧ�Դ��ڻ������ȡ��Һ���������ѡB��
�ʴ�Ϊ��16.3ml��B��
Ȼ��Ũ�������ձ��ڱڻ��������ձ��У����ò��������裬��ֹҺ��ɽ���
�ʴ�Ϊ����װ��ˮ���ձ��ڱڻ���ע��Ũ���ᣬ�ӱ߽��裻
3��ϴ��ҺҪת�Ƶ�100mL����ƿ�У��ʴ�Ϊ��100mL����ƿ��
4��������ˮע������ƿ����Һ��������ƿ�̶���1-2cm������ ��ͷ�ιܼ�ˮ��Һ����̶������У��Ǻ�ƿ�����������µߵ���ҡ�ȡ�
�ʴ�Ϊ����ͷ�ιܣ�
��2��A�����õ�Ũ���᳤ʱ��������ܷⲻ�õ������У�Ũ��������ˮ�ԣ��������ʵ����ʵ���ƫС��������Һ��Ũ��ƫ�ͣ�
B������ƿ������ϴ�Ӻ������������ˮ����Ӱ�����ʵ����ʵ�������Һ�����������������Һ�����ʵ���Ũ����Ӱ�졣
C�����ù����ձ���������δϴ�ӣ��������ʵ����ʵ���ƫС�����Ƶ���ҺŨ��ƫ�ͣ�
D������ʱ������Һ��Һ���棬������Һ�����ƫС������������Һ��Ũ��ƫ�ߡ�
�ʴ�Ϊ��ƫ�ͣ���Ӱ�죻ƫ�ͣ�ƫ�ߣ�
���������⿼����һ�����ʵ���Ũ����Һ�����ƣ��ѶȲ��������ȡŨ��������ѡ����Ͳ
�����Ѷȣ�һ��
5��ʵ���� ��10 �֣��������ʵ��װ��ͼ�ش����⣺
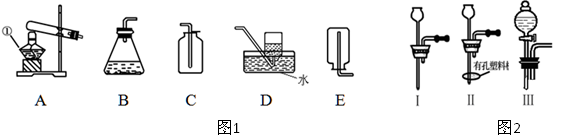
��1��ij����С���ͬѧ��ͼ1װ��̽��CO2��ʵ�����Ʒ���
�ټ�ͬѧ�ô���ʯ��ϡ���ᷴӦ��ȡCO2��Ӧ��ѡ�õķ���װ����??���ռ�װ����??��
�ڼ��ȹ���̼�����ƻ����̼����臨��ܲ���CO2���䷽��ʽ�ֱ��ǣ�
2NaHCO3 ?Na2CO3 + H2O +CO2��
?Na2CO3 + H2O +CO2��
NH4HCO3 ?NH3 ��+ H2O +CO2��
?NH3 ��+ H2O +CO2��
��ͬѧ���ü���̼�����Ƶķ�����ȡCO2��Ӧ��ѡ�õķ���װ����??????????��
����ѡ��̼�������ȡCO2��������???????????????????????????????????��
��2��ͼ1��װ��B��Ȼ������㣬�������Ʒ�Ӧ���ʡ����ͼ2��ѡȡ����������ţ�ȡ��B�еĵ��������Դﵽ���Ʒ�Ӧ���ʵ�Ŀ�ġ�
�ο��𰸣���1����B��2�֣� C��2�֣���A��2�֣�̼����識��ȷֽ��
�����������1���ٴ���ʯ�����ᷴӦ������Ҫ���ȣ�����ѡ��Bװ�á�CO2������ˮ�����ܶȴ��ڿ����ģ�����Ӧ���������������ռ�����ѡC��
������̼�����Ʒֽ���Ҫ���ȣ���̼�������ǹ��壬����Ӧ��ѡ��װ��A������̼����識��ȷֽ�����CO2��NH3�Ļ�����壬�Ӷ��Ƶõ�CO2���������Բ�ѡ��̼�������ȡCO2��
��2��Ҫ����Ʒ�Ӧ���ʣ������ѡ���Һ©������ѡ��װ�â�
�����Ѷȣ�һ��