微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8min间的平均反应速率和推测反应16min时反应物的浓度,结果应是( )
A.2.5?μmol?L-1?min-1和2.0?μmol?L-1
B.2.5?μmol?L-1?min-1和2.5?μmol?L-1
C.3.0?μmol?L-1?min-1和3.0?μmol?L-1
D.5.0?μmol?L-1?min-1和3.0?μmol?L-1

参考答案:由图可知,4~8 min期间,反应物浓度变化为(20-10)
本题解析:
本题难度:简单
2、填空题 (10分)在一定条件下,二氧化硫和氧气发生如下反应:
2SO2(g)+O2(g) 2SO3(g) ΔH<0
2SO3(g) ΔH<0
(1)写出该反应的化学平衡常数表达式K=__________。
(2)降低温度,该反应K值______,二氧化硫转化率______,化学反应速率______。(以上均填“增大”“减小”或“不变”)
(3)600 ℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图所示,反应处于平衡状态的时间是________。
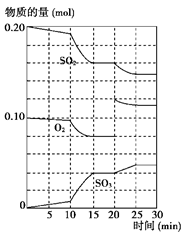
(4)据上图判断,反应进行至20 min时,曲线发生变化的原因是________________ _(用文字表达);10 min到15 min的曲线变化的原因可能是________(填写编号)。
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加SO3的物质的量
参考答案:(1) 本题解析:
本题解析:
试题分析:(1) 化学平衡常数是可能反应达到平衡状态时各生成物浓度幂指数的乘积与个反应物浓度的幂指数乘积的比,对该反应来说,其化学平衡常数表达式K=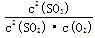 ;(2)由于该反应的正反应是放热反应,所以降低温度,平衡正向移动,该反应K值增大;二氧化硫转化率增大;降低温度,化学反应速率减小;(3)600 ℃时若反应处
;(2)由于该反应的正反应是放热反应,所以降低温度,平衡正向移动,该反应K值增大;二氧化硫转化率增大;降低温度,化学反应速率减小;(3)600 ℃时若反应处
本题难度:一般
3、选择题 将等质量的两份锌粉a和b,分别加入两个盛过量稀硫酸的烧杯中,并向加入a的烧杯中再加入少量CuO粉末。下列各图表示氢气体积V(H2)与反应时间t的关系,其中正确的是??
参考答案:A
本题解析:锌粉a由于置换铜,被部分消耗,所以最终生成的氢气略小,同时形成原电池,产生氢气的速率相对大。
本题难度:一般
4、选择题 C+CO2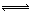 2CO;ΔH1>0,反应速率v1,N2+3H2
2CO;ΔH1>0,反应速率v1,N2+3H2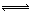 2NH3;ΔH2<0,反应速率v2。如升温,v1和v2的变化是 ( )
2NH3;ΔH2<0,反应速率v2。如升温,v1和v2的变化是 ( )
A.同时增大
B.同时减少
C.v1增大,v2减少
D.v1减少,v2增大
参考答案:A
本题解析:考查外界条件对反应速率的影响。温度升高反应速率一定增大,而与反应是放热还是吸热无关,也与平衡怎么移动无关。答案A。
本题难度:一般
5、选择题 下列对“化学反应速率”的理解正确的是
A.化学反应速率表示的是化学反应进行的限度
B.化学反应速率可以用单位时间内反应物浓度的减少量来表示
C.对于任何化学反应来说,反应速率越快,反应现象就越明显
D.化学反应速率可以是正值,也可以是负值
参考答案:B
本题解析:
试题分析:A、化学反应速率表示化学反应进行的快慢程度,不表示反应进行的限度,错误;B、化学反应速率可以用单位时间内反应物浓度的减少量来表示,也可以用单位时间内生成物浓度的增加量来表示,正确;C、反应速率与反应现象无关,错误;D、化学反应速率都是正值,无负值,错误,答案选B。
本题难度:一般